时间:2017-01-19 01:29:23
1、填空题 把AlCl3溶液蒸干灼烧,最后得到的主要固体产物是_________________,为什么?___________________(用化学方程式和必要的文字说明)。
参考答案:Al2O3;因为AlCl3是挥发性酸所形成的铝盐,加热促进A
本题解析:
本题难度:一般
2、选择题 弱酸酸式盐的酸根离子电离和水解并存,已知HSO3―电离大于水解。以NaHXO3表示NaHCO3和NaHSO3。对于NaHCO3和NaHSO3溶液,下列关系式中不正确的是(???)
A.c(Na+)+c(H+)=c(OH―)+c(HXO3―)+2c(XO32―)
B.c(Na+)= c(HXO3―)+ c(H2XO3)+c(XO32―)
C.c(Na+)> c(HXO3―)>c(H+)>c(OH―)
D.c(OH―)= c(H+)+ c(H2XO3)―c(XO32―)
参考答案:C
本题解析:
试题分析:C项:NaHSO3溶液呈酸性,说明溶液中HSO3-电离程度大于水解程度,c(H+)>>c(OH-),NaHCO3溶液呈碱性,说明HCO3-水解沉淀大于电离程度,c(OH-)>c(H+),故C错误。故选C。
点评:本题考查离子浓度的大小比较,题目难度较大,解答本题时注意从守恒的角度分析,本题中还要注意题目要求,即浓度均为浓度均为0.1mol?L-1的NaHSO3溶液和NaHCO3溶液中均存在的关系,此为解答该题的关键之处,注意审题。
本题难度:一般
3、填空题 (6分)常温下,已知pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合后,所得溶液显酸性;0.01mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性。请回答下列问题:
(1)高碘酸是????????(填“强酸”或“弱酸”)
(2)0.01mol/L的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合后所得溶液中,
c(IO3-)??????????c(Na+)(填“大于”、“小于”或“等于”)。
(3)已知某溶液中只存在OH-、H+、IO4-、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
A.c(Na+)>c(IO4-)>c(OH-)>c(H+)
B.c(IO4-)>c(Na+)>c(OH-)>c(H+)
C.c(Na+)>c(OH-)>c(IO4-)>c(H+)
D.c(IO4-)>c(Na+)>c(H+)>c(OH-)
填写下列空白:
①若溶液中只有一种溶质,则该溶质是?????????,上述四种离子浓度大小顺序为????????________(填选项的标号)
②若上述关系中C项是正确的,则溶液中的溶质有?????????、?????????
参考答案:本题解析:略
本题难度:一般
4、选择题 将标准状况下的2.24 L CO2通入150 mL 1mol / LNaOH溶液中,下列说法正确的是
A.c(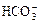 )略大于c(
)略大于c( )
)
B.该溶液只能与酸反应,不能与碱反应
C.c(Na+)等于c( )与c(
)与c(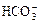 )之和
)之和
D.c(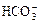 )略小于c(
)略小于c( )
)
参考答案:A
本题解析:略
本题难度:一般
5、选择题 根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 A.c(HCO3-)>c(ClO-)>c(OH-) B.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+C(OH-) C.c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) D.c(Na+)=c(HCO3-)+ c(CO32-) + c(H2CO3) +c(ClO-) +c(HClO) 参考答案:A 本题解析:c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+C(OH-) + 2c(CO32-) 本题难度:简单 |