时间:2017-01-19 01:23:09
1、实验题 某课外学习小组,为探究稀硝酸能与Cu反应生成无色的NO气体,设计了如下图所示的装置。请回答下列问题:
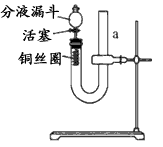
2、填空题 二氧化氯(ClO2)作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂.常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定.温度过高,二氧化氯的水溶液有可能爆炸.某研究小组设计如图所示实验制备ClO2.
(1)如图,在烧瓶中先放入一定量的KClO3和草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热.反应后产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为:______,
氧化产物与还原产物的物质的量之比为______.
(2)控制水浴温度在60~80℃之间的目的是______,
图示装置中缺少的一种必须的玻璃仪器是______.
(3)A装置用于吸收产生的二氧化氯,其中最好盛放______.(填序号)
①60℃的温水??②冰水????③饱和食盐水
(4)将二氧化氯溶液加入到硫化氢溶液中,所得溶液中加入少量氯化钡溶液,有白色沉淀生成.请写出二氧化氯溶液和硫化氢溶液反应的化学方程式______.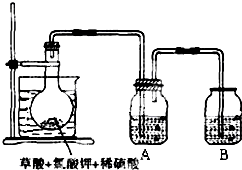
3、选择题 下述实验中不能达到预期实验目的的是(???????)???????????????????????????????
| 编号 | 实验内容 | 实验目的 |
| A | C2H5Cl和NaOH溶液混合后振荡再加入AgNO3溶液 | 检验C2H5Cl中的Cl元素 |
| B | 向沸腾的水中滴加FeCl3饱和溶液,继续煮沸至溶液呈红褐色为止 | 制备Fe(OH)3胶体 |
| C | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
| D | 室温下,用pH计测定浓度各为0.1mol/LNa2CO3溶液和CH3COONa溶液的pH | 比较H2CO3和CH3COOH的酸性强弱 4、实验题 经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。 5、实验题 研究性学习小组进行SO2的制备及性质探究实验。 |