时间:2017-01-19 01:23:09
1、实验题 (15分)氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN―等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
I.查阅资料:含氰化物的废水破坏性处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
II.实验验证:破坏性处理CN-的效果。
化学兴趣小组的同学在密闭系统中用图10装置进行实验,以测定CN-被处理的百分率,实验步骤如下: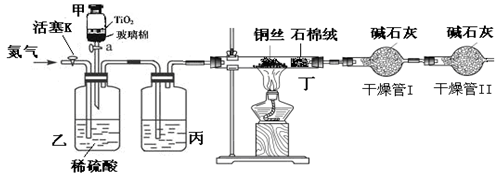
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol・L―1)倒入甲中,塞上橡皮塞。
步骤3:????????????????????????????????????
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式???????。
(2)完成步骤3?????????????。
(3)丙装置中的试剂是??????????,丁装置的目的是??????????????。
(4)干燥管Ⅱ的作用是????????????????????。
(5)请简要说明实验中通入N2的目的是?????????????。
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为??????。
参考答案:(1)2CNO―+6ClO―+8H+=2CO2↑+N2↑+C
本题解析:(1)次氯酸钠具有强氧化性,能把CNO―氧化生成氮气和CO2,所以反应式为2CNO―+6ClO―+8H+=2CO2↑+N2↑+Cl2↑+4H2O。
(2)由于需要通过加热的铜丝吸收氯气,所以应该先点燃丁处的酒精灯。
(3)因为生成的气体需要干燥,所以丙装置中应该盛放浓硫酸,干燥CO2气体。
(4)干燥管I是吸收CO2的,因此为了防止空气中的水和CO2进入干燥管I中影响对CO2的测量,需要再连接1个干燥管。
(5)由于装置中会残留部分CO2,所以通入氮气的目的是使装置中的CO2全部到干燥管I中被吸收,减少误差。
(6)干燥管Ⅰ中碱石灰增重1.408g,则反应中生成的CO2是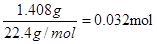 ,所以CNO―的物质的量是0.032mol。CN-的总的物质的量是0.04mol,所以根据原子守恒可知,该实验中测得CN-被处理的百分率为80%。
,所以CNO―的物质的量是0.032mol。CN-的总的物质的量是0.04mol,所以根据原子守恒可知,该实验中测得CN-被处理的百分率为80%。
本题难度:一般
2、选择题 下列实验操作和结论错误的是( ? )
A.用新制Cu(OH)2悬浊液可鉴别麦芽糖和蔗糖
B.用银镜反应可证明蔗糖是否转化为葡萄糖,但不能证明是否完全转化
C.浓H2SO4可使蔗糖变黑,证明浓H2SO4具有脱水性
D.蔗糖溶液中滴加几滴稀H2SO4,水浴加热几分钟,加入到银氨溶液中,不能发生银镜反应,证明蔗糖不水解
参考答案:D
本题解析:麦芽糖属于还原性糖,而蔗糖不是,A正确。B正确,产生银镜,只能说明水解生成来葡萄糖,但蔗糖是否剩余,则无法确定。浓硫酸具有脱水性,可使蔗糖炭化,C正确。发生银镜反应的条件是溶液显碱性,实验中没有用碱液中和硫酸是错误的。答案选D。
本题难度:简单
3、选择题 下列各组中两瓶无标签的无色溶液,不用其他试剂能鉴别出来的一组是( )
A.AlCl3和NaOH
B.NaHCO3和NaOH
C.Na2SO4和BaCl2
D.AgNO3和NaCl
参考答案:A.氯化铝溶液和氢氧化钠溶液,试剂添加顺序不同产生的现象不同
本题解析:
本题难度:一般
4、选择题 下列有关实验原理或操作正确的是?????????????????????????????????????
A.仅用硝酸银溶液便可鉴别亚硝酸钠和食盐
B.减压过滤是为了加快过滤速度,得到较大颗粒的晶体
C.硫酸亚铁铵晶体过滤后用无水乙醇洗涤
D.纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮
参考答案:C
本题解析:略
本题难度:一般
5、实验题 乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4・xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+???2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。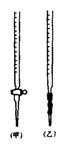
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;
请回答:
⑴ 滴定时,将KMnO4标准液装在右图中的?????(填“甲”或“乙”)滴定管中。
⑵ 本实验滴定达到终点的标志可以是???????????????????????????。
⑶ 通过上述数据,计算出x=?????????。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会??????(填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会??????。
参考答案:(1)甲(2)最后一滴高锰酸钾滴入溶液突然出现紫色(或紫红色
本题解析:略
本题难度:简单