时间:2017-01-19 01:01:37
1、选择题 对于体积相同的①(NH4) 2SO4、②NH4HSO4、③H2SO4溶液,下列说法正确的是(????)
A.溶液的pH相同时,3种溶液物质的量浓度大小顺序是③>②>①
B.溶液的pH相同时,将3种溶液稀释相同倍数,pH变化最大的是①
C.溶液的pH相同时,由水电离出的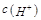 大小顺序是③>②>①
大小顺序是③>②>①
D.若3种溶液的物质的量浓度都相同,则溶液的pH大小顺序是①>②>③
参考答案:D
本题解析:硫酸铵水解显酸性,浓度最大,硫酸是强酸,浓度最小,A不正确。在稀释过程中,有利于水解,所以pH变化最大的是硫酸,B不正确。硫酸和硫酸氢铵均显强酸性,在pH相同的条件下,对水的抑制程度是相同的,C不正确。答案选D。
本题难度:简单
2、选择题 已知常温下,0.1mol/L的一元酸HA溶液的pH>1;0.1mol/L的一元碱MOH溶液中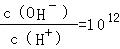 ,将此两种溶液等体积混合,混合夜中,离子浓度关系不正确的是( )
,将此两种溶液等体积混合,混合夜中,离子浓度关系不正确的是( )
A.c(OH﹣)=c(HA)+c(H+)
B.c(M+)>c(A﹣)>c(OH﹣)>c(H+)
C.c(A﹣)>c(M+)>c(H+)>c(OH﹣)
D.c(M+)+c(H+)=c(A﹣)+c(OH﹣)
参考答案:C
本题解析:
试题分析:0.1mol/L的一元酸HA溶液的pH>1,则酸部分电离,为弱酸;0.1mol/L的一元碱MOH溶液中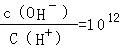 ,结合水的离子积常数知,
,结合水的离子积常数知,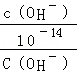 本题难度:一般
本题难度:一般
3、选择题 在室温下,等体积的酸和碱的溶液混合后,pH一定少于7的是
A.pH=3的醋酸跟pH=11的氢氧化钠溶液
B.pH=3的盐酸跟pH=11的氨水
C.pH=3硫酸跟pH=11的氢氧化钠溶液
D.pH=3的HNO3跟pH=11的KOH溶液
参考答案:A
本题解析:
试题分析:醋酸是弱酸,pH=3的醋酸溶液的浓度大于0.001mol/L,所以A中醋酸过量,溶液显酸性,pH小于7;同样分析,B中氨水过量,溶液显碱性,C和D中恰好反应,溶液显中性,答案选A。
点评:对于酸和碱中和后溶液酸碱性的判断,需要特别注意的是,不能首先判断生成的盐是否水解,而应该是先判断酸碱的过量问题。只有当酸碱恰好反应时,才能考虑生成的盐是否水解。
本题难度:一般
4、选择题 下列说法中正确的是
A.100mL pH=3的盐酸和醋酸溶液,与足量锌反应时,起始时二者产生氢气的速率醋酸快
B.100 mL 1 mol·L-1的盐酸和50 mL 2 mol·L-1的盐酸分别与足量的锌反应,两者放出氢气的速率和质量均相等
C.100 mL pH=3的盐酸和醋酸溶液,与足量锌反应后,所得氢气的质量醋酸多
D.100 mL 0.1mol·L-1的硫酸和盐酸溶液,与足量锌反应后,前者放出氢气的质量是后者放出氢气质量的2倍
参考答案:CD
本题解析:重点考查弱电解质的电离平衡及方程式计算。
A. pH=3相同的盐酸和醋酸溶液,H+浓度相同,与足量锌反应时,起始时二者产生氢气的速率醋酸相同。
B.100 mL 1 mol·L-1的盐酸和50 mL 2 mol·L-1的盐酸分别与足量的锌反应,由于两者的氢离子浓度不同,故反应速率不同;由于两者所提供氢离子的物质的量相同,两者放出氢气质量相等
CD均正确。
本题难度:一般
5、选择题 水的电离过程为H2O H++OH-,在25 ℃时水的离子积为KW=1.0×10-14,在35 ℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
H++OH-,在25 ℃时水的离子积为KW=1.0×10-14,在35 ℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
A.c(H+)随着温度的升高而降低
B.35 ℃时c(H+)>c(OH-)
C.35 ℃时的水比25 ℃时的水电离程度小
D.水的电离是个吸热过程
参考答案:D
本题解析:35 ℃时水的离子积大于25 ℃时水的离子积,说明35 ℃时水中c(H+)、c(OH-)大于25 ℃时水中c(H+)、c(OH-),但c(H+)仍等于c(OH-);亦说明升高温度,水的电离程度增大,即水的电离是吸热过程。
本题难度:一般