�����������е���ԭ��
�ο��𰸣�BC
�����������
�����Ѷȣ���
2��ʵ���� ��12�֣�ijѧ��Ϊ����֤������ԭ����ͭ�IJ���������ͼ��ʾ��ʵ��װ�á�
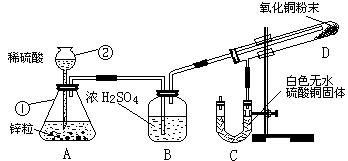
 ��д��������������ƣ���???????????? ��д��������������ƣ���????????????
��ŨH2SO4��������???????????????????????????????��
�DZ�ʵ����Ҫ���ȵ�װ��Ϊ???????������ĸ��ţ���
��д��װ��C��D�пɹ۲쵽������C ?????????????????��D????????????????????��
�� D�з�Ӧÿ����1��ˮ���ӣ�ת�Ƶĵ�����Ϊ?????????????����
�ο��𰸣�
 ����������� �����������
�����Ѷȣ�һ��
3��ʵ���� (16��)ij��Ȼ��Ļ�ѧ��ɿ���ΪaNa2CO3��bNaHCO3��cH2O(a��b��cΪ������)��Ϊȷ������ɣ���ѧ��ȤС���ͬѧ����������ʵ�飺
(1)���Է���
��ȡ������Ȼ����Ʒ�����Թ��У��þƾ��Ƽ��ȣ����Թܿ���Һ�����ɣ���Һ����ʹ��ˮ����ͭ�������ܷ�˵����Ʒ�к��ᾧˮ���Լ������ɡ�
���������һ����ʵ�鷽����ȷ����Ʒ�к���CO32�����ӡ�
(2)��������
��С��ͬѧ�������ͼ��ʾװ�ã��ⶨ��Ȼ��Ļ�ѧ��ɡ�
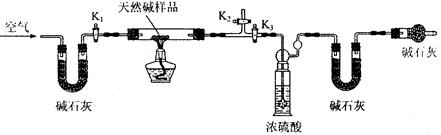
A?????????? B???????????????? C??????? D????????? E
ʵ�鲽�裺
�ٰ���ͼ(�г�����δ����)��װ��ʵ��װ�ú����Ƚ��еIJ�����????????????????��
A����ʯ�ҵ�������???????????????????????????????��
�ڳ�ȡ��Ȼ����Ʒ7.3g�����������Ӳ�ʲ������У�����װŨ�����ϴ��ƿ������Ϊ??? 87.6g��װ��ʯ�ҵ�U��D������Ϊ74.7g��
�۴���K1��K2���ر�K3������������������ӡ�
�ܹرջ���K1��K2����K3����ȼ�ƾ��Ƽ��ȣ������ٲ�������Ϊֹ��
�ݴ���K1������������������ӣ�Ȼ��Ƶ�װŨ�����ϴ��ƿ����Ϊ88.5g��װ��ʯ�ҵ�U��D������Ϊ75.8g���ò����л���������������ӵ�Ŀ����?????????????
?????????????????????????????????????????????????????????��
�����Ƶ���
����Ȼ��Ļ�ѧʽΪ????????????????????????????????????????��
�ο��𰸣�(1)���Է���
�ٲ���˵������Ϊ��Ȼ����Ʒ�еġ�NaH
�����������1����������Ȼ����Ʒ�еġ�NaHC03�����ȷֽ�Ҳ�ɲ���ˮ�����Բ���˵����
��Ҫ����CO32���������ó���������ȡ������Ȼ����Ʒ����ˮ������������CaCl2��Һ(��BaCl2��Һ)�����˲�ϴ�ӳ�����������м���ϡ���ᣬ������������ͨ������ʯ��ˮ�С����л�������˵����Ȼ����Ʒ�к���CO32-���ӡ�
��2����װ�����Ӻú�����Ҫ����װ�õ������ԡ����ڿ����к���ˮ������CO2�������ʵ�飬���Լ�ʯ�ҵ������dz�ȥͨ������е�CO2��H2O��
�����ڷ�Ӧ�в���������������װ���У�����ͨ�������������ʹ��Ӧ���ɵ�CO2��H2O��������ա�
��Ũ����ͼ�ʯ�ҷֱ����ӵ�������0.9g��1.1g������ˮ��CO2�����ʵ����ֱ���0.05mol��0.025mol������Ϊ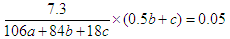 �� ��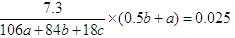
���a�Ub�Uc��1�U2�U1�����Ի�ѧʽΪNa2CO3��2NaHCO3��H2O��
�����Ѷȣ�һ��
4��ʵ���� ������ʵ��С���ͬѧΪ̽�������������������ķ�Ӧ����������ͼ��ʾ��װ�ý���ʵ�顣���������ľ�������Թ�D�У�ľ����ȼ��

��ش��������⣺
��1��д��װ��A�з�Ӧ�Ļ�ѧ����ʽ_____________________��
��2����1С��ͬѧͨ�����˼ά����ΪCװ���з��������·�Ӧ��2Na2O2��2SO2��2Na2SO3��O2����С��ͬѧ���˼ά��������ɷ���ʽ��_____________________��ʵ���У���ȥ��Bװ�ã���SO2ֱ�Ӻ�
Na2O2��Ӧ������֤��ʵ���в�����O2����SO2��Na2O2��Ӧ���ã�ԭ����_____________________��
��3�� ��2С��ͬѧ��ΪNa2O2��SO2��Ӧ��������Na2SO3��O2�⣬����Na2SO4���ɡ���2С��ͬѧ��������_____________________��
�ο��𰸣���1��Na2SO3+H2SO4==Na2SO4+SO2��+H
���������
�����Ѷȣ�һ��
5������� ��12�֣�ʵ������Ҫ500ml 0.4m ol��L-1��NaOH��Һ������ʱ�� ol��L-1��NaOH��Һ������ʱ��
��1������NaOH����ʱ������Ӧ����__________?????��������ƽ�����̳�����
��2�����ƹ����У����������п϶�����Ҫʹ�õ���???????????????????��
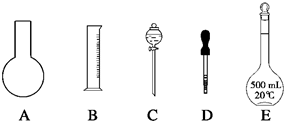
��3������ʵ���ʵ����Ҫ�ͣ�2�����г��������жϣ����ʵ�黹ȱ�ٵ������ǣ����������ƣ�______________________________??????????????????????????????????????????��
��4����ʵ��ʱ�������������������Һ��Ũ��ƫ�����?????????????��
A����ˮ����ʱ�����̶��ߣ�����������ˮ���̶���
B�����ǽ�ϴ��Һת������ƿ
C������ƿϴ�Ӻ��ڱ���ˮ���δ�����ﴦ��
D����Һδ��ȴ��ת������ƿ
E.����ʱ���ӿ̶���
�ο��𰸣���12�֣�ÿ��3�֣� ��1��?С�ձ�???��2�� A? C
�����������
�����Ѷȣ�һ��
|