时间:2017-01-19 00:26:10
1、选择题 下列关于晶体的说法一定正确的是(???)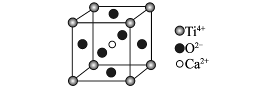
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶点)
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+与12个O2-相邻
C.SiO2晶体中每个硅原子与两个氢原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
参考答案:B
本题解析:有些单原子分子晶体中不存在共价键,如稀有气体构成的晶体,A错;因在晶体中Ti4+位于顶点而O2-位于面心,所以CaTiO3晶体中每个Ti4+与12个O2-相邻,B正确;SiO2晶体、Si原子与4个O原子以共价键结合,C错;金属晶体中有些比分子晶体的熔点低,如汞常温下为液体,D错。
本题难度:简单
2、选择题 下列物质的化学式可以表示真实的分子的是????????????????????(??? )
A.K2S
B.CO2
C.NaOH
D.SiO2
参考答案:B
本题解析:
试题分析:化学式能真实表示物质分子组成的是分子晶体,常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、据此即可解答。A、K2S为离子化合物,只有钾离子和硫离子,没有分子,故A错误;C、NaOH为离子化合物,只有钠离子和氢氧根离子,没有分子,故C错误;D、Si02为原子晶体,是由硅原子和氧原子以共价键构成的空间网状结构,没有Si02分子,故D错误。
故选B。
点评:本题主要考查分子晶体类型的
本题难度:一般
3、选择题 某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为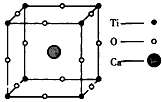 [???? ]
[???? ]
A.1:3:1
B.2:3:1
C.2:2:1
D.1:3:3
参考答案:A
本题解析:
本题难度:一般
4、选择题 同组物质中化学键类型相同、晶体类型也相同的是
A.Ar 、N2、 Si
B.金刚石、 O2、F2
C.Ba(OH)2、K2O 、CaCl2
D.NH3、CO2、CH4
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下列分子或离子的中心原子带有一对孤对电子的是[???? ]
A.HCl
B.BeCl2
C.CH4
D.PCl3
参考答案:D
本题解析:
本题难度:简单