时间:2017-01-17 23:52:07
1、选择题 三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热△H=-3677kJ/mol(P被氧化为P4O10),下列有关P4S3的说法中不正确的是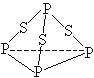
A.分子中每个原子最外层均达到8电子稳定结构
B.P4S3中硫元素为-2价磷元素为+3价
C.热化学方程式为P4S3( s)+8O2(g)=P4O10(s )+3SO2(g)△H=-3677kJ/mol
D.一个P4S3分子中含有三个非极性共价键
2、选择题 下列说法中不正确的是? [???? ]
A.有机化学作为一门学科萌发于17世纪,创立并成熟于18、19世纪
B.有机物都是共价化合物,它们不一定能溶于水
C.有机物都可以运用有机化学方法来合成
D.有机物中一定含有碳元素,但含碳元素的物质不一定是有机物
3、简答题 下列物质中,只存在离子键的是______,只存在共价键的是______;含离子键和非极性键的是______,属于离子化合物的是______,属于共价化合物的是______.(以上各空都填序号)
①N2②MgCl2③NH4Cl?④CH4⑤CO2⑥Ne?⑦H2S?⑧KOH?⑨Na2O2?⑩K2O.
4、选择题 烃类分子中的碳原子与其他原子的结合方式是[???? ]
A.形成四对共用电子对
B.通过非极性键
C.通过两个共价键
D.通过离子键和共价键
5、简答题 阅读下列信息:
Ⅰ、表中①~⑥为短周期元素及相应氢化物沸点的数据:
| 元素性质 | 元素编号 ① ② ③ ④ ⑤ ⑥ 氢化物的沸点(℃) -60.7 -33.4 100 -87.7 19.54 -84.9 最高化合价 +6 +5 +5 +7 最低化合价 -2 -3 -2 -3 -1 -1 A、B、Y均为上表中的元素. Ⅱ、X是一种历史悠久,应用广泛的金属元素. Ⅲ、X与Y可形成化合物XY、XY2,二者可用接触法制强酸甲. IV、A与B可形成化合物AB、AB2,二者均可用于制备强酸乙. 请回答: (1)写出一个表中所含电子数不同的氢化物之间的反应方程式______. (2)元素①氢化物的沸点低于元素______③氢化物的沸点,原因是______. (3)下列有关强酸甲、乙说法正确的是______. a.二者的浓溶液在常温时均可用X的单质制成容器储运 b.二者的浓溶液在敞口容器中放置,质量都会变化 c.工业生产强酸甲、乙时,都是用水吸收相应的氧化物 d.二者的稀溶液均为强氧化剂 (4)工业上生产强酸甲时可用浓氨水来源:91 考试网处理尾气,并获得某种正盐,其化学方程式为:______. (5)写出工业生产强酸乙的过程中获得AB的化学方程式:______,氧化剂与氧化产物的物质的量之比______,生成1molAB时转移的电子数______. | |||||