0.5mg・L-1
?
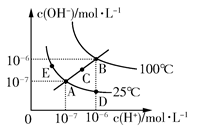
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=???????????mol・L-1。
(2)若酸性废水中Fe3+的浓度为1.0×10-4mol・L-1,c(AsO43-)=??????????mol・L-1。
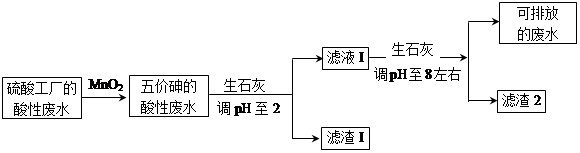
(3)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),MnO2被还原为Mn2+,反应的离子方程式为?????????????????????????????????????????????。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为?????????????;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,原因为???????????????????????????????
???????????????????????????????????????????????????????????????????????????。
③砷酸(H3AsO4)分步电离的平衡常数(25℃)为:K1=5.6×10-3?K2=1.7×10-7?K3=4.0×10-12,第三步电离的平衡常数的表达式为K3=???????????????????????????。Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O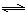 HAsO42-+OH-,该步水解的平衡常数(25℃)为:??????????????????(保留两位有效数字)。 HAsO42-+OH-,该步水解的平衡常数(25℃)为:??????????????????(保留两位有效数字)。
3、选择题 下列热化学方程式中的△H能表示可燃物的燃烧热的是[???? ]
A.H2(g)+ Cl2(g)=2HCl(g) △H=-184KJ・mol-1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802.3J・mol-1
C.CO(g)+1/2O2(g)=CO2(g) △H=-293KJ・mol-1
D.2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ・mol-1
4、选择题 下列说法或表示方法正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)=C(金刚石) 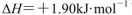 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定
C.一定条件下,将0.5 mol N2(g)和1.5 molH2 (g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: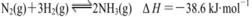
D.在稀溶液中,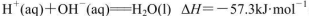 ,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ ,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ
5、选择题 25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是 [???? ]
A.C(s)+1/2O2(g)=CO(g) △H= -393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(l) △H= +571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= -890.3 kJ/mol
D.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H= -2800 kJ/mol
|