时间:2017-01-17 21:45:33
1、填空题 X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的结构式为____________。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+997 mol·L-1 b.+297 mol·L-1 c.-206 mol·L-1 d.-2418 kJ·mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:______________;由R生成Q的化学方程式:_______________________________________________。
参考答案:(1)O;第三周第ⅢA族;Al>C>N>O>H
(2
本题解析:
本题难度:一般
2、选择题 某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3∶1。用石墨电极电解该溶液时,依据电极产物,可明显分为三个阶段。下列叙述不正确的是(???)
A.阴极只析出H2
B.阳极先析出Cl2,后析出O2
C.电解最后阶段为电解水
D.溶液的PH值不断增大,最后为7
参考答案:D
本题解析:由两种溶质NaCl和H2SO4的物质的量之比为3∶1,电解时可将分为三个阶段:⑴电解HCl阶段,⑵电解NaCl阶段,⑶电解H2O阶段。有电解的原理可知,始终阴极上析出的为H2,阳极在⑴、⑵段析出Cl2,⑶段析出O2,在⑵段产生了NaOH,PH值大于7。
本题难度:简单
3、选择题 用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为(??? )
A.阳极100g,阴极128g
B.阳极93.6g,阴极121.6g
C.阳极91.0g,阴极119.0g
D.阳极86.0g,阴极114.0g
参考答案:B
本题解析:
试题分析:根据题意知,用铜作电极电解硝酸银溶液时,阳极上铜失电子发生氧化反应,电极反应式为Cu-2e-=Cu?2+,阴极上银离子得电子生成银,电极反应式为Ag++e-=Ag,设阴极析出银的质量为x,阳极溶解铜的质量为y,根据电子守恒得x/108=2y/64,两个电极质量差为溶解铜的质量和析出银的质量之和,所以x+y=28,解得x=21.6,y=6.4。所以阳极上金属质量=100g-6.4g=93.6g,阴极上金属质量=100g+21.6g=121.6g,选B。
本题难度:一般
4、填空题 (16分)四种短周期元素A、B、C、D的性质或结构信息如下。
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题。
(1)①C元素在周期表中的位置?????????, 请写出BC2分子的电子式____________。
②A元素的单质与物质甲发生反应的离子方程式___________________。
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式。负极__________;正极(2)A所在周期中, E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,
X、Y都是惰性电极,实验开始时,同时在两边各滴入
几滴酚酞试液,则
①电解池中Y极上的电极反应式????????????????。
检验Y电极反应产物的方法是???????????
②电解一段时间后,若阴极收集到112ml标准状况下的气体,
此时电解液的PH为??????(假设电解液的体积保持不变,常温下)
参考答案:16分,每空2分) 本题解析:略 本题难度:一般 5、选择题 15.有机电解制备的金属醇盐,可直接作为制备纳米材料的前体。以下是一种电化学合成金属醇盐的主要装置。 参考答案:CD 本题解析: 本题难度:一般
(1)①第2周期ⅥA族?;??
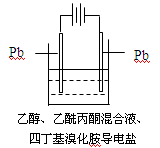
在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
2CH3CH2OH+2e-=2CH3CH2O-+H2↑
2CH3COCH2COCH3+2e—=2(CH3COCHCOCH3)+H2↑
下列说法正确的是
A.阳极Pb失去电子,发生还原反应
B.当阳极失去2 mol e—时,阴极产生2 mol氢气
C.电解过程中,阳离子向阴极移动
D.已知Pb-4e—=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol
试题分析:A项阳极Pb失去电子,发生氧化反应;B项根据电极反应2CH3CH2OH+2e-=2CH3CH2O-+H2↑,阳极失去2mole-时,阴极产生1molH2;C项电解过程中,阳离子向阴极移动;D项根据电极反应Pb-4e—=Pb4+,当消耗Pb的质量为207g时,转移电子是4mol,当消耗Pb的质量为103.5g时,转移电子2mol。
考点:原电池和电解池的工作原理
点评:本题考查学生电解池的工作原理及电子守恒的计算,难度中等。