时间:2017-01-17 10:42:01
1、选择题 下列说法正确的是( )
A.溶度积常数大者,溶解度也大
B.由于AgCl水溶液导电性很弱,所以它是弱电解质
C.难溶电解质离子浓度的乘积就是该物质的溶度积常数
D.难溶电解质的溶度积常数与温度有关
参考答案:A、因同一类型的沉淀,溶度积常数大者,溶解度也大,不同类型的
本题解析:
本题难度:简单
2、选择题 用0.1mol・L-1 AgNO3溶液分别滴定20.00mL浓度均为 0.1mol・L-1 Cl-、Br-、I-溶液,以滴入的AgNO3溶液体积为横坐标, pX为纵坐标[pX=-lgc(X-),X=Cl-、Br-、I-],可绘得下图滴定曲线。已知25℃时: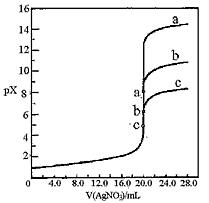

有关说法不正确的是 [???? ]
A.用硝酸银滴定法测定试样中c(Cl-),可滴加0.1mol・L-1 K2CrO4 溶液1~2滴作指示剂
B.a、b、c依次分别表示Cl-、Br-及I-
C.向NaCl和NaBr的混合溶液中滴加硝酸银溶液, 当两种沉淀共存时,c (Br-)/c(Cl-) =2.7×10-3
D.若用硝酸银溶液滴定NaI溶液,当pX=13时, 溶液中c (Ag+)≈0.64×10-17
参考答案:BD
本题解析:
本题难度:一般
3、填空题 七水硫酸镁(MgSO4・7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1?部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 | ||||||||||||||||||
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 ? 表2?两种盐的溶解度(单位为g/100g水)
|