时间:2017-01-17 10:37:23
1、选择题 下列说法中无科学性错误的是????
A.离子晶体中一定无共价键
B.极性分子中一定无非极性键
C.非极性分子中一定无极性键
D.分子晶体中一定无离子键
2、填空题 在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ,现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为
(注:某反应物的转化率=该反应物转化(消耗)的物质的量÷该反应物起始的物质的量×100%)
3、填空题 (18分)实验是化学学习的基础,请完成以下实验填空:
Ⅰ.(1)常压下,已知甲烷的热值是55.625KJ/g,请写出甲烷燃烧热的热化学方程式 。
(2)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。若实验中大约要使用245 mL NaOH溶液,配制0.50 mol/L NaOH溶液时至少需要称量NaOH固体 g。
(3)测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。装置中环形玻璃搅拌棒的搅拌方法是 ,该实验过程中量筒最少要准备 个。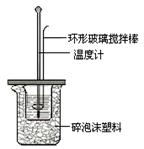
(4)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①下表中的a= ℃
| 温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | |||||||||||||||||||||||||||||
| H2SO4 | NaOH | 平均值 | ||||||||||||||||||||||||||||||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | a | |||||||||||||||||||||||||||
| 2 | 27.0 | 27.4 | 27.2 | 31.3 | ||||||||||||||||||||||||||||
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | ||||||||||||||||||||||||||||
| 4 | 26.4 | 26.2 | 26.3 | 31.4 ②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c="4.18" J/(g・℃)。则中和热△H= (取小数点后一位)。 ③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母) 。 a.实验装置保温、隔热效果差 b.量取NaOH溶液的体积时仰视读数 c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中 d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 e、配置氢氧化钠溶液的氢氧化钠固体中混有氧化钠 Ⅱ.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题: (1)硫酸铜溶液可以加快氢气生成速率的原因是_______________________________; (2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| ||||||||||||||||||||||||||||