时间:2017-01-17 10:36:04
1、选择题 相同温度下,100mL0.01mol/L的NH3?H2O与10mL0.1mol/L的NH3?H2O相比较,下列数值前者大于后者的是( )
A.c(H+)
B.c(OH-)
C.电离程度
D.中和时所需HCl的量
参考答案:A.相同温度下,0.01mol/L的NH3?H2O小于0.1
本题解析:
本题难度:一般
2、选择题 下列有关说法正确的是 ( )
A.TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加
B.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
C.pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为强碱
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
参考答案:A
本题解析:
试题分析:A、根据△G=△H―T・△S可知,△G<0时反应自发。如果TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加,即△S>0,A正确;B、氯化钠是强酸强碱盐,不水解,溶液显中性。醋酸铵是弱酸弱碱盐,酸根离子与铵根离子水解程度相同,溶液显中性,但促进水的电离,B不正确;C、pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为弱碱,碱过量,溶液显碱性,C不正确;D、Na2CO3溶液中加入少量Ca(OH)2固体生成碳酸钙沉淀和氢氧化钠,CO32-水解程度减小,但溶液的碱性增强,pH增大,D不正确,答案选A。
考点:考查反应自发性、水的电离、盐类水解以及溶液酸碱性判断
本题难度:一般
3、选择题 相同条件下,等体积、等pH的醋酸溶液和盐酸分别加水稀释后,溶液的pH仍相同,则所得溶液的体积
A.仍相同
B.醋酸溶液的大
C.盐酸的大
D.无法判断
参考答案:B
本题解析:
试题分析:盐酸是强酸,醋酸是弱酸,当pH相同时,醋酸浓度大,稀释过程中,电离平衡右移,H+浓度减小程度小,稀释后pH仍相同,醋酸加水多,选B。
考点:考查弱电解质的电离。
本题难度:一般
4、填空题 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表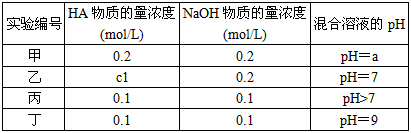
请回答下列问题:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA 是强酸还是弱酸
?____________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2 mol/L______? (填“是”或“否”)。混合溶液中离子浓度c(A-)与c(Na+)的大小关系是________。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是______酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是
________________________________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=_________mol/L。写出该混合溶液中下列算式的精确结果(不能做近似计算)。 c(Na+)-c(A-)=________mol/L
参考答案:(1)如a=7,HA为强酸,如a>7,则为弱酸
本题解析:
本题难度:一般
5、选择题 室温下向一定量的稀氨水中加入水稀释后,下列说法正确的是(??)
A.因为稀释,溶液中所有离子的浓度均减小
B.溶液中[c(H+)・c(NH3・H2O)]/ c(NH4+)不变
C.NH3・H2O的电离程度增大,c(OH-)亦增大
D.再加入与氨水等体积等浓度的盐酸,混合液pH=7
参考答案:B
本题解析:
试题分析:A、因为稀释温度不变,Kw不变,溶液中C(OH-)减小,故C(H+)会增大,错误;B、溶液中[c(H+)・c(NH3・H2O)]/ c(NH4+)为一水合氨的电离常数,温度不变,电离常数不变,正确;C、NH3・H2O的电离程度增大,但由于溶液的体积增大,c(OH-)减小,错误;D、再加入与氨水等体积等浓度的盐酸,二者恰好完全反应,所得溶液为氯化铵溶液,水解显酸性,pH<7,错误。
本题难度:一般