时间:2017-01-17 09:49:36
1、选择题 泰雅紫是古代地中海沿岸出产的一种贵重染料,罗马帝王用法律规定,只有皇族与教主可穿用这种染料染的紫色衣袍.当时人们是从小的紫蜗牛中提取泰雅紫的,制备1.5g泰雅紫需要多达12000只紫蜗牛,现知其结构为如下图所示的含溴有机化合物,下列说法不正确的是???( )
A.泰雅紫分子的分子式为:C16H8N2Br2O2
B.1mol泰雅紫与H2加成最多需9molH2
C.泰雅紫属于烃的衍生物
D.检验泰雅紫中溴元素可直接加入硝酸银溶液,观察是否有浅黄色沉淀生成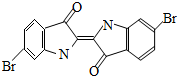
2、选择题 下列说法正确的是 [???? ]
A.含有金属元素的化合物一定是离子化合物
B.IA族和VIIA族元素原子化合时,一定生成离子键
C.由非金属元素形成的化合物一定不是离子化合物
D.活泼金属与活泼非金属化合时,能形成离子键
3、选择题 下列选项错误的是[???? ]
A.在NH4Cl晶体中含有离子键和共价键
B.设想把“H2+ Cl2=2HCl”设计成燃料电池,用于工业制盐酸,并进行发电
C.某反应△H >0,△S >0,该反应是个非自发反应
D.25℃时,NaNO2溶液的pH =8,c(Na+) -c(NO2-)= 9.9×10-7mol/L
4、选择题 关于晶体的下列说法正确的是(????)
①在晶体中只要有阴离子就一定有阳离子,只要有阳离子就一定有阴离子;②分子晶体的熔点一定比金属晶体的低;③晶体中分子间作用力越大,分子越稳定;④离子晶体中,一定存在离子键;⑤分子晶体中,一定存在共价键;⑥原子晶体中,一定存在共价键;⑦熔融时化学键没有破坏的晶体一定是分子晶体??
A.②④⑥
B.④⑤⑦
C.④⑥⑦
D.③④⑦
5、简答题 短周期主族元素A、B、C、D、E、F的原子序数依次增大.A和B形成4个原子核的分子,A和C形成3个原子核的分子,且两种分子均含有10个电子.D的阳离子电子层结构与氖相同,且与A同主族.E的常见氧化物有两种,其中一种能使品红溶液褪色.
(1)F在周期表中的位置是第______周期第______族.
(2)①C和D可形成原子个数比为1:1的化合物甲,甲是______(填“离子”或“共价”)化合物,电子式是______.
②D和E能形成离子化合物,用电子式表示该化合物的形成过程______.
(3)M是一种常见的金属单质,与元素F的单质转化关系如下图所示: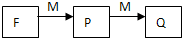
P→Q反应的离子方程式是______.
(4)E与F可形成一种相对分子质量是135的共价化合物乙.乙在橡胶硫化时,可以做硫的溶剂,乙遇到水时可以反应生成三种中学常见物质,其中一种是使品红溶液褪色的E的氧化物,一种是黄色固体.
乙和水反应的化学方程式是______.