时间:2017-01-16 15:56:23
1、选择题 某溶液中存在Na+、 、
、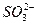 、Cl-、
、Cl-、 、Br-中的若干种,依次进行下列实验:
、Br-中的若干种,依次进行下列实验:
(1)用pH试纸检验,溶液的pH>7;
(2)向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈橙色,用分液漏斗分液;
(3)向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液,只有白色沉淀产生,过滤;
(4)在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生。
下列判断正确的是(??? )
①肯定有Na+②肯定有 ③肯定有
③肯定有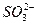
④肯定有Br-⑤肯定有Cl-⑥肯定没有
A.①③④⑥
B.①②④⑥
C.②③④⑥
D.③④⑤⑥
2、选择题 在下列离子方程式中正确的是
A.醋酸和小苏打溶液反应:H++HCO3-=CO2↑+H2O
B.硫氢化钠的水解:HS-+H2O=H3O++S2-
C.铁与三氯化铁溶液反应:Fe+Fe3+=2Fe2+
D.铝与氢氧化钠溶液反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
3、选择题 某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A.Na+
B.CO32-、NH4+
C.CH3COO-
D.CH3COO-、Na+
4、选择题 下列物质混合后,不能发生离子反应的是( )
A.硫酸钠溶液和氯化钡溶液
B.硝酸钠溶液与氯化钾溶液
C.稀硫酸滴到铜片上
D.稀盐酸和碳酸钠溶液
5、选择题 下列各组物质混合后,既产生无色气体,又产生白色沉淀的是
①Ba(NO3)2溶液跟NaHSO3溶液,②Ba(OH)2溶液跟(NH4)2SO4溶液共热,③电石跟苏打水,④三氯化铁溶液跟碳酸氢钠溶液.
A.①②③
B.②③
C.①②③④
D.①③