ʱ��:2017-01-16 15:27:55
1������� ��14�֣�NH3��һϵ�з�Ӧ���Եõ�HNO3��NH4NO3������ͼ��ʾ��
��1�����У�NH3��O2�ڴ��������·�Ӧ���仯ѧ����ʽ��_______________________��
��2�����У�2NO(g)��O2(g) 2NO2(g)��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)���¶ȱ仯������(��ͼ)��
2NO2(g)��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)���¶ȱ仯������(��ͼ)��
�ٱȽ�p1��p2�Ĵ�С��ϵ�� ��
�����¶����ߣ��÷�Ӧƽ�ⳣ���仯�������� ��
��3�����У������¶ȣ���NO2(g)ת��ΪN2O4(l)�����Ʊ�Ũ���ᡣ
����֪��2NO2(g) N2O4(g)��H1 2NO2(g)
N2O4(g)��H1 2NO2(g) N2O4(l) ��H2
N2O4(l) ��H2
���������仯ʾ��ͼ�У���ȷ����(ѡ����ĸ) ��
��N2O4��O2��H2O���ϵĻ�ѧ����ʽ�� ��
��4�����У����NO�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��
Ϊʹ������ȫ��ת��ΪNH4NO3���貹��A��A�� ��˵�����ɣ� ��
�ο��𰸣���14�֣�
��1��4NH3��5O2���������
�����������1�����ڴ�������������������Ӧ����NO��ˮ���仯ѧ����ʽ��4NH3��5O2 4NO��6H2O��
4NO��6H2O��
��2����2NO(g)��O2(g)  2NO2(g)���÷�Ӧ�����������С�Ŀ��淴Ӧ������ѹǿ��ƽ�������ƶ���NO��ƽ��ת�������ߣ�����p1��p2�Ĵ�С��ϵΪp1��p2���������¶ȣ�NO��ƽ��ת���ʽ��ͣ�˵��ƽ�������ƶ����������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ڷ��ȷ�Ӧ�������¶ȣ���ѧ��Ӧƽ�ⳣ����С��
2NO2(g)���÷�Ӧ�����������С�Ŀ��淴Ӧ������ѹǿ��ƽ�������ƶ���NO��ƽ��ת�������ߣ�����p1��p2�Ĵ�С��ϵΪp1��p2���������¶ȣ�NO��ƽ��ת���ʽ��ͣ�˵��ƽ�������ƶ����������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ڷ��ȷ�Ӧ�������¶ȣ���ѧ��Ӧƽ�ⳣ����С��
��3����2NO2(g) N2O4(g)��H1��2NO2(g)
N2O4(g)��H1��2NO2(g) N2O4(l)��H2���Ƿ��ȷ�Ӧ����Ӧ������������������������Cͼ����ͬһ������̬ʱ����������Һ��ʱ��������Aͼ��ȷ��Bͼ����ѡA��
N2O4(l)��H2���Ƿ��ȷ�Ӧ����Ӧ������������������������Cͼ����ͬһ������̬ʱ����������Һ��ʱ��������Aͼ��ȷ��Bͼ����ѡA��
��N2O4��O2��H2O��Ӧ�������ᣬ���ϵĻ�ѧ����ʽ��2N2O4��O2��2H2O===4HNO3��
��3�����ݵ��ʾ��ͼ��֪�����NO�Ʊ�����泥�������ӦΪ��NO-3e-+2H2O=NO3-+4H+��������ӦΪ��NO+5e-+6H+=NH4++H2O����������Ӧ�ɿ�����Ҫʹ���ӵ�ʧ�غ㣬����������NO3-������������������NH4+�������ܷ�ӦΪ8NO��7H2O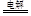 3NH4NO3��2HNO3��Ӧ���������İ�����������Ϊ���ݷ�Ӧ8NO��7H2O
3NH4NO3��2HNO3��Ӧ���������İ�����������Ϊ���ݷ�Ӧ8NO��7H2O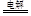 3NH4NO3��2HNO3����������HNO3�ࡣ
3NH4NO3��2HNO3����������HNO3�ࡣ
���㣺���黯ѧ��Ӧ����д��Ӱ�컯ѧƽ������أ���ѧͼ��ķ���������Ӧ�á�
�����Ѷȣ�����
2��ѡ���� ��ˮ�м�������ʵ�����Ag����Pb2����K����SO42����NO3����Cl�����ö��Ե缫������Һ�����ռ����������������������뻹ԭ���������֮��Ϊ��???����
A��35.5:108
B��16:207
C��108:35.5
D�� 8:1
�ο��𰸣�D
���������
����������������ӷ�Ӧ������������֪����ˮ�м�������ʵ�����Ag����Pb2����K����SO42����NO3����Cl���������Ȼ���������Ǧ��ɫ����������Һʵ��ʱ�������Һ�����Ե���ʵ��ʱ�ǵ��ˮ��������������������ԭ���������������ߵ�����֮��Ϊ16�U2����ѡD��
����������Ĺؼ������ȸ������ӹ��棬�ó���Һ�д��ڵ��������ӣ�Ȼ�����жϼ��ɡ��������׳��ֵ������ǣ�ֱ���������ӵķŵ�˳���ж���������ͻ�ԭ����Ӷ��ó�����Ľ��ۡ������������֪ʶ������Ҫ�ġ�
�����Ѷȣ�һ��
3��ѡ���� ���ӣ�Ni-Cd���ɳ�������ִ��������й㷺Ӧ�á���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�Cd?+?2NiO(OH)?+?2H2O Cd(OH)2?+?2Ni(OH)2�йظõ�ص�˵����ȷ����
Cd(OH)2?+?2Ni(OH)2�йظõ�ص�˵����ȷ����
A�����ʱ������Ӧ��Ni(OH)2??+?OH-?-e-==?NiO(OH)+?H2O
B���������ǻ�ѧ��ת��Ϊ���ܵĹ���
C���ŵ�ʱ����������Һ�ļ��Բ���
D���ŵ�ʱ�������Һ�е�OH-�������ƶ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� ��14�֣������ҹ����Ԫ�أ�Ҳ���۵���ߵĽ���������Ϊ������ʹ�ߡ����ú��ٿ�[FeWO4��MnWO4(WΪ+6��)]����������������ߴ��ٵĻ����������¡���֪H2WO4�Dz�����ˮ�����ᣬ���ȿɷֽ������������ش������й����⣺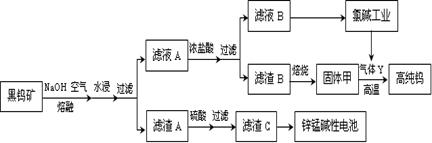
��1������������ͨ�������Ŀ���� ��
��2������A�����ᷴӦ�����ӷ���ʽΪ ��
��3��ʵ������п�̼��Ե��������Դģ���ȼҵ��װ������ͼ��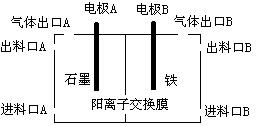
��֪��п�̼��Ե�ص��ܷ�ӦΪZn+2MnO2+2H2O=Zn(OH)2+2MnOOH����п�̼��Ե�ص�п�缫Ӧ��װ���е缫 (�A����B��)��ӣ�����YΪ������� ���A����B�������������壬Ϊ�������Ч�ʣ���ʼʱ���ӽ��Ͽ�B���������Ϊ ��д��п�̼��Ե��������Ӧʽ ��
��4����֪������̼Ҳ���������Ƶ��٣�������Y�����õ���̼��ԭ�� ��
��5����H2��CO2��4:1������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4����֪��
CH4 (g) + 2O2(g)  CO2(g)+ 2H2O��1�� ��H1����890.3 kJ/mol
CO2(g)+ 2H2O��1�� ��H1����890.3 kJ/mol
H2(g) + 1/2O2(g)  H2O��1�� ��H2����285.8 kJ/mol
H2O��1�� ��H2����285.8 kJ/mol
��CO2(g)��H2(g)��Ӧ����CH4(g)��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
�ο��𰸣���14�֣�
�� ����Fe2����Mn2����2�֣�
���������
�����������1����Ϊп�̼��Ե���к��ж������̣�����ͨ�������Ŀ��������Fe2����Mn2����ʹ��ת��ΪFe3+��Mn4+��
��2����Ϊ�������ӱ�����Ϊ�����ӣ����������Ʒ�Ӧ�������������������ڼ��������£�����ת��Ϊ����������������������������A��ϡ���ᷴӦʵ������������ϡ���ᷴӦ�����ӷ���ʽ��Fe2O3 + 6H��= 2Fe3�� + 3H2O �� Fe3O4 + 8H��= 2Fe3��+ Fe2��+ 4H2O��
��3������п�̵�ص�Zn����������Ӧ����ԭ��صĸ�������ҺA�����ᷴӦ����������������շֽ�����WO3���ȼҵ�в������������������������������ɻ�ԭWO3ΪW�������ڸ�����������Fe����������������Fe��Ϊ����������п�̼��Ե�ص�п�缫Ӧ��װ���е缫B��������������B�ڳ��������壻Ϊ��ǿ��Һ�ĵ����ԣ��ڽ��Ͽ�B������ϡNaOH��Һ������п�̵�ص�����������ԭ��Ӧ���������̵õ���������MnOOH���缫��ӦʽΪMnO2 + e��+ H2O =" MnOOH" + OH����
��4������̼���ʻ�ԭWO3����W�п��ܺ���C���ʣ�����������ԭ����������ʣ�
��5�����ø�˹���ɽ�������ȥ������CO2(g)��H2(g)��Ӧ����CH4(g)��Һ̬ˮ�ķ�Ӧ�Ȧ�H=4��H2-��H1=��252.9kJ/mol������CO2(g)��H2(g)��Ӧ����CH4(g)��Һ̬ˮ�ĵ��Ȼ�ѧ����ʽ��CO2(g)+4H2(g)=CH4(g)+2H2O(l)��H=��252.9kJ/mol��
���㣺���鹤ҵ���̵ķ������绯ѧ��Ӧԭ����Ӧ�ã���˹���ɵ�Ӧ��
�����Ѷȣ�����
5��ѡ���� ��ʯīΪ�缫���ϵ��ʱ������˵����ȷ����[???? ]
A�����NaOH��Һʱ����ҺŨ�Ƚ���С��pH����
B�����H2SO4��Һʱ����ҺŨ�Ƚ�����pH����
C�����Na2SO4��Һʱ����ҺŨ�Ƚ�����pH����
D�����NaCl��Һʱ����ҺŨ�Ƚ���С��pH����
�ο��𰸣�C
���������
�����Ѷȣ�һ��