ʱ��:2017-01-16 15:19:20
1��ѡ���� �������ʵ�ת���ڸ�����������ʵ�ֵ���
��Fe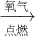 Fe2O3
Fe2O3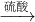 Fe2��SO4��3
Fe2��SO4��3
��SiO2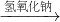 Na2SiO3
Na2SiO3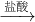 H2SiO3
H2SiO3
��AlCl3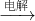 Al
Al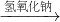 NaAlO2
NaAlO2
��Na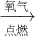 Na2O
Na2O NaOH
NaOH
��SO2 H2SO3
H2SO3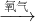 H2SO4��
H2SO4��
A.�٢�
B.�ڢ�
C.�ڢ�
D.�ۢ�
�ο��𰸣�C
���������������������������Ӧ����������������
�ڶ���������������Ʒ�Ӧ���ɹ����ƺ�ˮ�������ƺ����ᷴӦ���ɹ�����Ȼ��ƣ�
���Ȼ��������ǹ��ۻ��������⣻
���ƺ������ڵ�ȼ�������£����ɹ������ƣ�
�ݶ��������ˮ��Ӧ���������ᣬ�������������Ӧ�������
��𣺢�����������Ӧ3Fe+2O2 Fe3O4���ò���Fe2O3���ʢٴ���
Fe3O4���ò���Fe2O3���ʢٴ���
�ڶ���������������Ʒ�Ӧ2NaOH+SiO2�TNa2SiO3+H2O�������ƺ����ᷴӦNa2SiO3+2HCl=H2SiO3��+2NaCl���ʢ���ȷ��
���Ȼ��������ǹ��ۻ�����ɷ��ӹ��ɣ������ӣ�����⣬���Եò��������ʢ۴���
���ƺ������ڵ�ȼ�������£����ɹ������ƣ�2Na+O2 Na2O2���ò��������ƣ��ʢܴ���
Na2O2���ò��������ƣ��ʢܴ���
�ݶ��������ˮ��ӦSO2+H2O?H2SO3���������������Ӧ2H2SO3+O2�T2H2SO4���ʢ���ȷ��
��ѡC��
���������⿼����Ԫ�ػ���������ʣ���Ϥ��صĻ�ѧ��Ӧ�ķ���ʽ�ǽ��Ĺؼ�����Ŀ�ϼ�
�����Ѷȣ�һ��
2������� I��ijͬѧ���ʵ�齫Fe3O4��CuO��ɵĻ����X������ͼ��ʾ��ת����ÿһ������Ӧ��ȫ��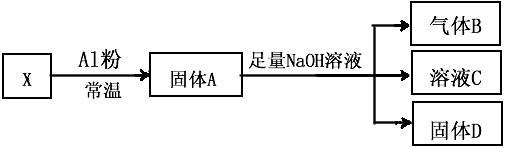
��1����������B�Ļ�ѧ����ʽ��____________________________��
��2��������DͶ�����ϡ���Ტ��ַ�Ӧ���ˣ�������Һ����˫��ˮ���û�ɫ��Һ�� д��������˫��ˮʱ��Һ�з�����Ӧ�����ӷ���ʽ��________________________ ��
��3������֪����X������Ϊ7��2g��Ӧ��Al�۵�������2��7g������B�ڱ�״���µ����Ϊ672mL�������D��������____________ g��
II�������A��̼���ƺ�̼��������ɡ���������������ȵĻ����A��
��4����������һ������100mL 3mol/L��Ba(OH)2��Һ����������ʹHCO3-��CO32-ȫ����Ϊ���������˺�������Һ�м���200mL 2mol/L��ϡ���ᣬ��Һǡ�ó����ԡ�
��д�����з�Ӧ�����ӷ���ʽ
̼��������������������ķ�Ӧ��____________________________��
�ڻ����A��NaHCO3������Ϊ____________________g��
��5��������һ�����ȼ�50mL8mol/L��HCl��Һ��ʹHCO3-��CO32-ȫ����ΪCO2���ټ�50mL2mol/L��
Ba(OH)2��Һ����Ϻ����ҺpH=14����Ϻ���Һ����仯���Բ��ơ��ڳ����£��������A��Na2CO3������Ϊ_______________g��
�ο��𰸣���1��2Al+2NaOH+2H2O==2NaAlO2+3H2
���������
�����Ѷȣ�һ��
3��ѡ���� ʵ������Al2(SO4)3��ȡAl(OH)3������ʵ��Լ���
A��NaOH
B��H2SO4
C��NH3?H2O
D��KOH
�ο��𰸣�C
���������
�������������Bѡ����������ȡAl(OH)3����A��D����ǿ������Ƕ�ӻ����ټӶ���ʹ��������ȫ������������Կ������Ӽ��������Cѡ��ֻ�谱ˮ����������ʹ��������ȫ�������ʴ�ѡC��3��
����������ؼ����ڷ����������������ԣ���������ȡʱ����ʹ��ǿ�
�����Ѷȣ�һ��
4������� ij����С���һЩ�������ʺͻ���������ʽ����о���
��1���±�Ϊ�������Ȼ�ͭ��Һ��Ӧ��ʵ�鱨���һ���֣�
| ʵ�鲽�� | ʵ������ |
| �ٽ���ĥ������Ƭ������������һ��Ũ�ȵ�CuCl?2��Һ�С� | �������ݣ��������ɵĺ�ɫ���壬��Һ��Ϊ��ɫ�� |
| �ڷ�Ӧ������������Һ���á� | ? |
| �ۺ�ɫ����������ˮϴ�Ӻ����ڳ�ʪ�����С� | һ��ʱ�������ɺ�ɫ��Ϊ��ɫ[������Ҫ�ɷ�ΪCu2(OH)2CO3]�� ? ��ʵ���з�����Ӧ������д�����л�ѧ����ʽ�������ӷ�Ӧ��ֻд���ӷ���ʽ�� ���������ɵĺ�ɫ����????????????????????????????????????????????????�� ��һ��ʱ�������ɺ�ɫ��Ϊ��ɫ??????????????????????????????????????�� ��2����ʯī���缫���������ʵ����������Һ�������������ݡ�������⣬��������������Һ�л��ɹ۲쵽��������????????????????????????????????????????????????????????????????????????????�� ���ʹ���������ӷ���ʽ��???????????????????????????��????????????????????????????????�� ��3����ҵ�Ͽ����������̿���Ҫ�ɷ�ΪMnO2����Ӧ�����������̡� �����������̿�ұ���̵�ԭ���ǣ��û�ѧ����ʽ��ʾ�� ???????????????????????????????????????????????????????????????????�� ��MnO2��H2O2�ֽⷴӦ������������������MnO2�����ữ���H2O2��Һ�У�MnO2�ܽ����Mn2+���÷�Ӧ�����ӷ���ʽ��???????????????????????????????????????????????????????????????????�� �ο��𰸣���1����2Al+3Cu2+=2Al3++3Cu??????�� ��������� �����Ѷȣ�һ�� 5������� п�ᣨH2ZnO2���β�ͬ�����ᣨH3AlO3���Σ�п�����ȶ����ڣ���п���ƣ�Na2ZnO2�����������ȶ�������ת��Ϊƫ�����Σ��������Ӧ������ƫ�����ƣ�NaAlO2�������������ƣ�Na3AlO3���� �ο��𰸣���1��2NaOH+Al2O3�T�T2NaAlO2+H2O �����������1��Al2O3��NaOH��aq��������Ӧ��2NaOH+Al2O3�T�T2NaAlO2+H2O �����Ѷȣ�һ�� |