时间:2017-01-15 17:04:26
1、选择题 下列说法正确的是[???? ]
A.常温下,向pH为1的硝酸溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
B.Al3+、NO3-、Cl-、CO32-、Na+可以大量共存于pH=2的溶液中
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同
2、选择题 在下列给定条件的水溶液中,一定能大量共存的离子组是( )
A.含有大量SiO2-3的溶液:K+、Na+、OH-、Cl-
B.使石蕊变红的溶液:Fe2+、Na+、NO-3、SO2-4
C.含有大量Al3+的溶液:I-、K+、S2-、NO-3
D.使酚酞变红的溶液:Ca2+、NH+4、HCO-3、Cl-
3、选择题 在下述条件下,一定能大量共存的离子组是
[?????]
A.无色透明的水溶液中:K+ 、Ba2+、I-、MnO4-
B.含有大量NO3-的水溶液中:NH4+ 、Fe2+、SO42-、H+
C.c(HCO3-)=0.1mol・L-1的溶液中:Na+ 、K+、CO32-、Br-
D.强碱性溶液中:ClO-、S2-、HSO3-、Na+
4、选择题 下列微粒在水溶液中能大量共存的是
A.Fe3+、H+、I-、Na+
B.Al3+、Na+、AlO2-、SO42-
C.K+、NH4+、H+、CO32―
D.Cu2+、SO42―、Al3+、Cl―
5、选择题 在一瓶PH=1的无色溶液中,已检验出含有Ba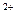 、Ag
、Ag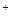 ,则下列粒子:①Cl
,则下列粒子:①Cl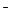 、②Mg
、②Mg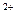 、③Cu
、③Cu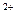 、④ NO
、④ NO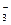 、⑤AlO2―、⑥ CO
、⑤AlO2―、⑥ CO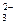 、⑦NH3・H2O在此溶液中不能大量存在的正确组合是
、⑦NH3・H2O在此溶液中不能大量存在的正确组合是
A.①②③⑥⑦
B.②③⑤⑥⑦
C.①③⑤⑥⑦
D.①②⑤⑥⑦