±Φδ:2017-01-15 16:48:43
1ΓΔ Β―ιΧβ (12Ζ÷)Ρ≥Μ·―ßΩΈΆβΜνΕ·–ΓΉι―–ΨΩ““¥Φ―θΜ·ΒΡ Β―ι≤Δ―ι÷ΛΤδ≤ζΈοΘ§…ηΦΤΝΥΦΉΓΔ““ΝΫΧΉΉΑ÷Ο(ΆΦ÷–ΒΡΦ–≥÷“«ΤςΨυΈ¥Μ≠≥ωΘ§ΓΑΓςΓ±±μ ΨΨΤΨΪΒΤ»»‘¥)Θ§ΟΩΧΉΉΑ÷Ο”÷Ω…Μ°Ζ÷ΈΣΔΌΓΔΔΎΓΔΔέ»ΐ≤ΩΖ÷ΓΘ“«Τς÷– ΔΖ≈ΒΡ ‘ΦΝΈΣΘΚaΓΣΈόΥ°““¥Φ(Ζ–ΒψΘΚ78Γφ)ΘΜbΓΣΆ≠ΥΩΘΜcΓΣΈόΥ°ΝρΥαΆ≠ΘΜdΓΣ–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΓΘ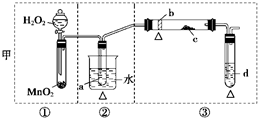
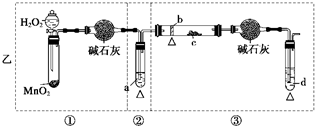
(1)Φρ ωΝΫΧΉΖΫΑΗΗςΉ‘ΒΡ”≈ΒψΘΚ
ΦΉΘΚ__________________________________________________________________Θ§
““ΘΚ___________________________________________________________________ΓΘ
(2)Φ·÷–ΝΫΧΉΖΫΑΗΒΡ”≈ΒψΘ§Ήι≥…“ΜΧΉ±»ΫœΚœάμΆξ…ΤΒΡ Β―ιΉΑ÷ΟΘ§Ω…Α¥ΤχΝς”…Ήσ÷Ν”“ΒΡΥ≥–ρ±μ ΨΈΣ_________________________________________________________(άΐ»γΦΉΔΌΘ§““ΔΎ)ΓΘ
(3)»τ“Σ±Θ÷Λ¥Υ Β―ι”–ΫœΗΏΒΡ–ß¬ Θ§ΜΙ–η≤Ι≥δΒΡ“«Τς”–________Θ§άμ”…_______________ΓΘ
(4) Β―ι÷–Ρή―ι÷Λ““¥Φ―θΜ·≤ζΈοΒΡ Β―ιœ÷œσ «________________________________ΓΘ
(5)ΉΑ÷Ο÷–Θ§»τ≥Ζ»ΞΒΎΔΌ≤ΩΖ÷Θ§ΤδΥϋ≤ΌΉς≤Μ±δΘ§‘ρΈόΥ°ΝρΥαΆ≠ΈόΟςœ‘±δΜ·Θ§Τδ”ύœ÷œσ”κ(4)œύΆ§Θ§ΆΤΕœ»Φ…’Ιή÷–÷ς“ΣΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ__________________________________ΓΘ
≤ΈΩΦ¥πΑΗΘΚ(1)ΦΉΘΚΔΌ÷–”ΟΖ÷“Κ¬©ΕΖΩ…“‘ΩΊ÷Τ“ΚΧεΒΡΝςΝΩΘ§ΩΊ÷ΤΖ¥”ΠΒΡΫχ––ΘΜ
±ΨΧβΫβΈωΘΚ(1)Φρ ωΝΫΧΉΖΫΑΗΗςΉ‘ΒΡ”≈ΒψΘΚ
ΦΉΘΚΔΌ÷–”ΟΖ÷“Κ¬©ΕΖΩ…“‘ΩΊ÷Τ“ΚΧεΒΡΝςΝΩΘ§ΩΊ÷ΤΖ¥”ΠΒΡΫχ––ΘΜΔΎ÷–”Ο»»Υ°‘ΓΦ”»»Θ§Ω…–Έ≥…ΫœΤΫΈ»ΒΡ““¥ΦΤχΝςΘ§ ΙΖ¥”ΠΗϋ≥δΖ÷ΘΜΔΎ÷–ΒΡ–±ΓΔ≥ΛΒΦΙήΤπΒΫάδΡΐΜΊΝς““¥Φ’τΤχΒΡΉς”ΟΓΘ
““ΘΚΔΌ”κΔέ÷–ΒΡΗ…‘οΙήΩ…Ζά÷Ι»ή“Κ÷–ΒΡΥ°”κΈόΥ°ΝρΥαΆ≠Ζ¥”ΠΘ§±ήΟβΗ…»≈…ζ≥…ΈοΒΡ―ι÷Λ
(2)Φ·÷–ΝΫΧΉΖΫΑΗΒΡ”≈ΒψΘ§Ήι≥…“ΜΧΉ±»ΫœΚœάμΆξ…ΤΒΡ Β―ιΉΑ÷ΟΘ§Ω…Α¥ΤχΝς”…Ήσ÷Ν”“ΒΡΥ≥–ρ±μ ΨΈΣ: ““ΔΌΘ§ΦΉΔΎΘ§““Δέ
(3)»τ“Σ±Θ÷Λ¥Υ Β―ι”–ΫœΗΏΒΡ–ß¬ Θ§ΜΙ–η≤Ι≥δΒΡ“«Τς”–Έ¬Ε»ΦΤ, άμ”… «ΩΊ÷ΤΥ°‘ΓΈ¬Ε»‘Ύ78ΓφΜρ¬‘ΗΏ”Ύ78ΓφΘ§ Ι““¥Φ’τΤχΤΫΈ»Νς≥ωΘ§Φθ…ΌΜ”ΖΔΘ§ΧαΗΏΖ¥”Π–ß¬ ΓΘ
(4) Β―ι÷–―ι÷Λ““¥ΦΒΡ―θΜ·≤ζΈοΒΡ Β―ιœ÷œσ «ΘΚc¥ΠΈόΥ°ΝρΥαΆ≠±δάΕΘΜd¥Π…ζ≥…Κλ…Ϊ≥ΝΒμ
(5) ‘ρΈόΥ°ΝρΥαΆ≠ΈόΟςœ‘±δΜ·Θ§Τδ”ύœ÷œσ”κ(4)œύΆ§Θ§ΆΤΕœ»Φ…’Ιή÷–÷ς“ΣΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
C2H5OHCuΓςCH3CHOΘΪH2Γϋ
±ΨΧβΡ―Ε»ΘΚΦρΒΞ
2ΓΔ―Γ‘ώΧβ œ¬Ν– Β―ιΉΑ÷Ο «ΧΫΨΩΆ≠ΥΩ”κΙΐΝΩ≈®ΝρΥαΒΡΖ¥”ΠΘ§œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «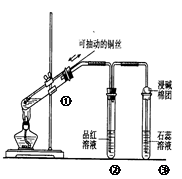
AΘ°ΉΑ÷ΟΔΌΡήΩΊ÷ΤΖ¥”ΠΒΡΖΔ…ζΚΆΫα χ
BΘ°»τΫΪΖ¥”ΠΚσΔΎΒΡ ‘Ιή»Γœ¬Θ§‘ΎΆ®Ζγ≥ς÷–Φ”»»Θ§Μα≤ζ…ζ¥ΧΦΛ–‘ΤχΈΕΒΡΤχΧεΘ§»ή“Κ≥ Κλ…Ϊ
CΘ°Δέ÷– ·»ο»ή“Κ±δΚλ…Ϊ
DΘ°ΈΣ»Ζ»œCuSO4…ζ≥…Θ§œρΔΌ÷–Φ”Υ°Θ§Ιέ≤λ»ή“Κ―’…Ϊ
≤ΈΩΦ¥πΑΗΘΚD
±ΨΧβΫβΈωΘΚΆ≠ΚΆ≈®ΝρΥαΖ¥”Π…ζ≥…SO2ΓΔΝρΥαΆ≠ΚΆΥ°ΓΘSO2»ή”ΎΥ°œ‘Υα–‘Θ§Ρή Ι ·»ο ‘“Κœ‘Κλ…ΪΘ§Υυ“‘―ΓœνABCΕΦ «’ΐ»ΖΒΡΓΘD≤Μ’ΐ»ΖΘ§”ΠΗΟ «Α― ‘Ιή÷–ΒΡ»ή“ΚΒΙ»κΥ°÷–Θ§“ρΈΣ ‘Ιή÷–ΜΙΚ§”–≈®ΝρΥαΘ§¥πΑΗ―ΓDΓΘ
±ΨΧβΡ―Ε»ΘΚΦρΒΞ
3ΓΔ―Γ‘ώΧβ œ¬ ω Β―ι≤ΜΡή¥οΒΫ‘ΛΤΎΡΩΒΡΒΡ «????????????????????????????????????????????????????????????Θ®???Θ©
| ±ύΚ≈ | Β―ιΡΎ»ί | Β―ιΡΩΒΡ | |
| A | ΫΪSO2Ά®»κΥα–‘KMnO4»ή“Κ÷– | ÷ΛΟςSO2ΨΏ”–Τ·ΑΉ–‘ | |
| B | ΫΪCl2Ά®»κNaBr»ή“Κ÷–Θ§»ΜΚσΦ”»κCCl4Θ§’ώΒ¥ΓΔΨ≤÷Ο | ±»Ϋœ¬»”κδεΒΡ―θΜ·–‘«Ω»θ | |
| C | ΫΪΆ≠Τ§Ζ÷±π”κ≈®ΓΔœΓœθΥαΖ¥”Π | ΧΫΨΩ≈®ΓΔœΓœθΥα―θΜ·–‘ΒΡœύΕ‘«Ω»θ | |
| D | œρ Δ”–20g’αΧ«ΒΡ…’±≠÷–Φ”»κΦΗΒΈΥ°Θ§ΫΝΑηΨυ‘»ΓΘ‘ΌΦ”»κ…Ό–μ≈®ΝρΥαΘ§―ΗΥΌΫΝΑηΓΘ | ΧΫΨΩ≈®ΝρΥαΒΡΆ―Υ°–‘ ≤ΈΩΦ¥πΑΗΘΚA ±ΨΧβΫβΈωΘΚ―ΓœνA «ΈΣΝΥ÷ΛΟςSO2ΨΏ”–ΜΙ‘≠–‘ΓΘ ±ΨΧβΡ―Ε»ΘΚΦρΒΞ 4ΓΔ Β―ιΧβ ΔώΓΘ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»»ή“ΚΒΡ≈δ÷ΤΚΆΥαΦν÷–ΚΆΒΈΕ® «÷–―ßΜ·―ß÷–ΝΫΗωΒδ–ΆΒΡΕ®ΝΩ Β―ιΓΘΡ≥―–ΨΩ–‘―ßœΑ–ΓΉι‘Ύ Β―ι “÷–≈δ÷Τ1mol/LΒΡœΓΝρΥα±ξΉΦ»ή“ΚΘ§»ΜΚσ”ΟΤδΒΈΕ®Ρ≥Έ¥÷Σ≈®Ε»ΒΡNaOH»ή“ΚΓΘœ¬Ν–”–ΙΊΥΒΖ®÷–’ΐ»ΖΒΡ «______________Θ®¥πΑΗΩ…Ρή≤ΜΈ®“ΜΘ© ≤ΈΩΦ¥πΑΗΘΚΔώ Θ® ?Ι≤16Ζ÷Θ© Θ®3Ζ÷Θ©? AΓΔBΓΔDΓΘ????(Εύ―Γ ±ΨΧβΫβΈωΘΚ¬‘ ±ΨΧβΡ―Ε»ΘΚ“ΜΑψ 5ΓΔΧνΩ’Χβ Θ®12Ζ÷Θ© |