时间:2017-01-15 16:42:47
1、填空题 请回答关于氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______;
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为
①Na2CO3溶液 ②HCl(盐酸)③BaCl2溶液,这三种试剂添加的合理顺序是______________(填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。 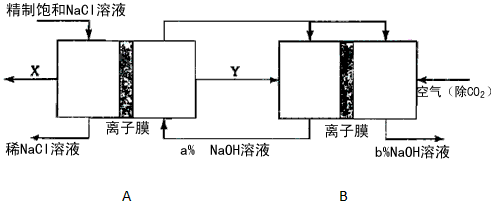
图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小
_________; 分别写出燃料电池B中正极、负极上发生的电极反应正极:_____________; 负极:
_______________;这样设计的主要节(电)能之处在于(写出1处)______________________;
(4)现有200mL食盐水,其中含有少量的NaOH,该溶液的pH等于10,用石墨电极电解,当阴极产生的气体体积为0.224L(标准状况)时停止电解。阳极的电极反应式_______________________。电解后溶液的pH约为(忽略溶液的体积变化)______________。
2、填空题 请回答氯碱的如下问题
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=____________(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是________________(填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。 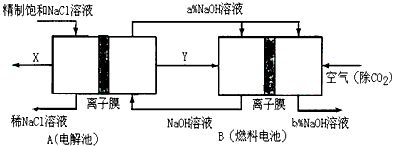
①图中X、Y分别是______________、_______________(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小___________________;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:_____________;负极:____________;
③这样设计的主要节(电)能之处在于(写出2处)_________________、___________________。
3、填空题 (三选一)【选修2:化学与技术】
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前,以下“技术”中,可用于“海水淡化”的是_________???(填序号)。
①蒸馏法?????②膜分离法(电渗析、反渗透)?????③冷冻法?????④离子交换法
(2)海水晒盐利用的化学原理是________;分离食盐晶体后的母液中含有________,经过分离、提纯后,可用于___________。???
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应的离子方程式为_________;电解所用的食盐水需要精制,为什么??__________________;精制时所用试剂为:盐酸、BaCl2溶液、NaOH溶液、Na2CO3溶液。加入试剂时,Na2CO3溶液必须在加入________之后加入。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下: 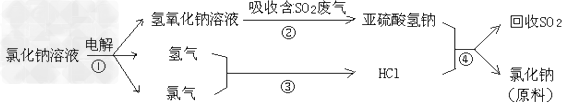
写出反应②的化学方程式_____________。
4、简答题 氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:
(1)精制过程中反应的离子方程式为______.
(2)电解过程的总反应方程式为______.
(3)电解槽阳极产物可用于______(至少写出两种用途).
(4)已知NaOH、NaCl在水中的溶解度数据如下表:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 NaOH/g 109 118 129 146 177 300 313 318 337 NaCl/g 36 36.3 36.6 37 37.3 37.8 38.4 39 39.8 根据上述数据,脱盐的主要工序应为______、______.脱盐后的碱液含NaOH约50%,含NaCl仅约2%左右,NaCl能够从溶液中大量析出的原因是______. 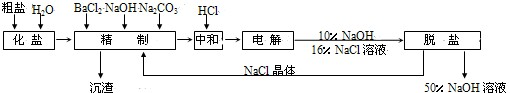 5、选择题 下列关于工业生产的说法中正确的是[???? ] |