时间:2017-01-15 15:18:53
1、选择题 燃烧2 g乙醇(液态),生成二氧化碳气体和液态水,经测定放出的热量为Q kJ,则乙醇燃烧的热化学方程式书写正确的是
A.C2H5OH(l)+3O2(g)====2CO2(g)+3H2O(l) ΔH=-23Q kJ・mol-1
B.C2H5OH(l)+3O2(g)====2CO2(g)+3H2O(l) ΔH=-Q/23 kJ・mol-1
C.1/2 C2H5OH(l)+3/2O2(g)====CO2(g)+3/2H2O(l) ΔH=-Q kJ・mol-1
D.C2H5OH(l)+3O2(g)====2CO2(g)+3H2O(l) ΔH=+23Q kJ・mol-1
参考答案:A
本题解析:燃烧2 g乙醇(液态),生成二氧化碳气体和液态水,经测定放出的热量为Q kJ,则燃烧1 mol液态乙醇生成二氧化碳和液态水的反应热为:ΔH="-23Q" kJ・mol-1,故乙醇燃烧的热化学方程式为:C2H5OH(l)+3O2(g)====2CO2(g)+3H2O(1) ΔH="-23Q" kJ・mol-1。
本题难度:简单
2、选择题 在强酸溶液中存在大量的Fe2+和Ba2+,那么在溶液中含有的离子是
A.NO3-
B.SO42-
C.Cl-
D.CO32-
参考答案:C
本题解析:分析:在强酸溶液中存在大量的Fe2+和Ba2+,则具有氧化性的离子以及与Ba2+反应生成沉淀的离子不能大量共存.
解答:A.酸性条件下Fe2+与NO3-发生氧化还原反应,故A错误;
B.Ba2+与SO42-反应生成沉淀而不能都可共存,故B错误;
C.Cl-与Fe2+和Ba2+以及氢离子都不反应,可大量共存,故C正确;
D.酸性条件下CO32-不能大量共存,故D错误.
故选C.
点评:本题考查离子共存问题,综合考查学生元素化合物知识的应用能力,为高考常见题型,题目难度不大,注意常见离子的性质以及反应类型.
本题难度:简单
3、选择题 下列说法或表示方法正确的是
A.反应物的总能量低于生成物的总能量时,该反应一定不能发生
B.在10l kPa、25 ℃时,1 g H2完全燃烧生成气态水,放出120.9 kJ的热量,则氢气的燃烧热为241.8 kJ/mol
C.已知:2SO2 (g) + O2 (g)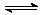 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
D.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) ;△H<0
参考答案:D
本题解析:
试题分析:A、反应物的总能量低于生成物的总能量为吸热反应,有可能发生,错误;B、燃烧热为1mol燃料完全燃烧,生成稳定的产物时得反应热,所以生成气态水的反应热不是燃烧热,错误;C、因为SO2与O2的反应为可逆反应,1 mol SO2和0.5 mol O2不可能完全反应,放出的热量要小于49.15kJ;D、石墨比金刚石稳定,说明石墨的能量低于金刚石,所以金刚石转化为石墨为放热反应,△H<0,正确。
本题难度:一般
4、填空题 (12分) 2SO2(g)+O2(g)
参考答案:
本题解析:
本题难度:一般
5、填空题 (14分)A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、
D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶
液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图 ,E元素在周期表中的位置是 。
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为 。
(3)D与C按原子个数比为1:1形成化合物的电子式是 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是 (填具体的化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与 C形成的化合物甲反应的离子方程式 。
(6)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl―NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式: ;放电时溶液中H+移向 (填“正”或“负”)极。
(7) E(s)+O2(g) EO2(g) △H1 E(g)+O2(g) EO2(g) △H2,则△Hl △H2(填“>”或“<”或“=”)。
参考答案:(共14分)(1)本题解析:
试题分析:(1)A、B组成的气态化合物的水溶液呈碱性,所以A是H元素,B是N元素,二者形成的化合物是氨气,水溶液呈碱性;A、[D都能与C按原子个数比为1:1或2:1形成化合物,则D是Na,C是O,形成的化合物氧化物与过氧化物均是原子个数比为1:1或2:1,E与C的最外层电子数相同,则E是S元素。D的原子结构示意图是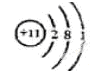 ,E在元素周期表则的位置是第三周期第VIA族;
,E在元素周期表则的位置是第三周期第VIA族;
(2)A与C形成原子个数比为1:1的化合物甲是过氧化氢,化学键类型是共价键;
(3)D与C按原子个数比为1:1形成化合物是过氧化钠,属于离子化合物,电子式为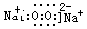 ;
;
(4)N的非金属性比O弱,所以B、C所形成氢化物水的稳定性大于氨气,稳定性由强到弱的顺序是H2O、NH3;
(5)F金属投入到盐酸溶液中,生成了浅绿色溶液M,则M是氯化亚铁,F是Fe,氯化亚铁与过氧化氢在酸性条件下发生氧化还原反应,生成铁离子和水,离子方程式为2Fe2++H2O2+2H+=2Fe3++H2O;
(6)以氢气、氮气为原料的电池的正极是氮气发生还原反应,结合电解质溶液氮气得电子与氢离子结合生成铵根离子,电极反应式为N2+6e-+8H+=2NH4+;原电池中的阳离子移向正极,所以放电时溶液中H+移向正极;
(7)固体熔化为液体需要吸热,所以气态S完全燃烧放出的热量多,则△Hl>△H2
考点:考查元素的判断,元素及其化合物的性质应用,电化学反应原理、热效应的判断
本题难度:一般