时间:2017-01-15 15:11:38
1、选择题 下列实验操作会导致实验结果偏低的是
①配制100 g 10%的CuSO4溶液,称取10 g硫酸铜晶体溶于90 g水中?②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮.③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为0.2 g,所得溶液的浓度.④用酸式滴定管量取用98%,密度为1.84 g/cm3的浓H2SO4配制200mL 2 mol・L-1的稀H2SO4时,先平视后仰视
A.只有①
B.只有②?
C.②③④
D.①③④
参考答案:D
本题解析:10 g硫酸铜晶体中硫酸铜的质量小于10g,浓度偏低。②中所用的晶体已经受潮,说明水的含量高,测定结果偏高。③中药品与砝码放反了,游码读数为0.2 g,则药品的质量大于砝码的质量减去0.2g,因此质量偏低,浓度偏低。滴定管仰视读数则实际量取的体积偏小,测定结果偏低,答案选D。
本题难度:一般
2、选择题 下列有关实验操作中,正确的是
A.用试管取出试剂瓶中的NaOH溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.银镜反应实验后的废液可先倒入水槽中,再用水冲入下水道
C.向试管中滴加液体时,胶头滴管必须紧贴试管内壁,避免液体溅出
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
参考答案:D
本题解析:
试题分析:A、实验室取用化学药品一般不能放回原瓶,错误;B、实验过程中产生的废液应放置在废液桶中,不能随便倒掉,错误;C、胶头滴管应垂直滴加,不能靠在器皿壁上造成污染,错误;D、正确。
本题难度:一般
3、选择题 下列叙述正确的是
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B.当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处
C.制取并排水法收集氧气结束后,应立即停止加热
D.将含硫酸的废液倒入水槽,用水冲人下水道
参考答案:B
本题解析:
试题分析A、少量浓硫酸不慎滴到皮肤上,可以用大量水冲洗,再用3%~5%的NaHCO3溶液涂上,故A不正确;B、CO易于血红蛋白结合从而是人体失去氧而中毒,所以当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处,故B正确;C、制取并排水法收集氧气结束后,如果立即停止加热,容易引起液体倒流,故C错误;D、硫酸是强酸,不能随意排放,随意将含硫酸的废液倒入水槽,用水冲人下水道是错误的,故D不正确,答案选B。
本题难度:一般
4、实验题 信息时代产生的大量电子垃圾对环境构成了极大的威胁。某化学兴趣小组将一批废弃的线路板简单处理后,得到主要含Cu、Al及少量Fc、Au、Pt等金属的混合物,设计了如下制备硫酸铜晶体和硫酸铝晶体的路线: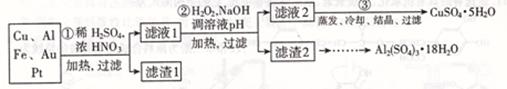
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
| 沉淀物 | Fe( OH)2 | Fe( OH)3 | ? Al( OH)3 | Cu( OH)2 |
| 开始沉淀 | 5.8? | 1.1 | 4.0 | ? 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2? | ? 6.7 ??? 请回答下列问题: (1)第①步操作前需将金属混合物进行粉碎,其目的是?????????????????????????????; (2)某学生认为用H2O2代替浓HNO3更好,理由是???????????????????????????????????; 请写出Cu溶于H2O2与稀硫酸混合溶液的离子方程式是?????????????????????????????????。 (3)第②步中应将溶液pH调至?????????????????。 (4)由滤渣2制取Al2( SO4)3.18H2O,探究小组设计了两种方案: 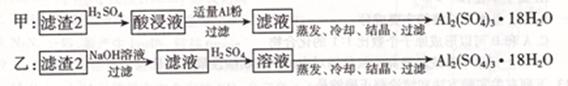 你认为????????种方案为最佳方案,理由是??????????????????、?????????????????。 (5)为了测定硫酸铜晶体的纯度,某同学准确称取4.0g样品溶于水配成l00mL溶液,取l0m溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.l000mol・L-1Na2S2O3标准溶液滴定至终点,共消耗14. 00mL Na2S2O3标准溶液。上述过程中反应的离子方程式如下: 2Cu2+ +4I-=2CuI(白色)↓+I2??? 2S2O 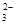 +I2= 2I-+S4O +I2= 2I-+S4O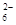 ①样品中硫酸铜晶体的质量分数为____????????????。 ②另一位同学提出通过测定样品中硫酸根离子的量也可求得硫酸铜晶体的纯度,其他同学认为此方案不可行,理由是?????????????????????????。 参考答案: 本题解析: 本题难度:困难 5、选择题 下列说法正确的是 ?? [???? ] A.用托盘天平进行称量,一般可准确到0.01 g B.容量瓶上标有温度和容量,使用前要检查是否漏水 C.配制硫酸溶液时,可先在量筒中加入一定体积的水,再慢慢注入浓硫酸 D.用四氯化碳、苯或酒精均可以从溴水中萃取溴 参考答案:B 本题解析: 本题难度:简单 |