时间:2017-01-13 11:18:09
1、实验题 (15分)某研究性小组设想将少量Cl2通入Fe2+和I-的混合溶液中,探究Fe2+和I-的还原性强弱。
[提出假设]
假设1:Fe2+的还原性比I-强
假设2:I-的还原性比Fe2+强
假设1:一样强
[验证假设]
(1)设计如下几种装置进行实验:
实验必须的装置是A→_______________(按Cl2气流方向的顺序填写)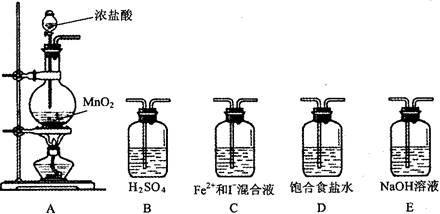
(2)实验开始后,控制通入少量Cl2,通过观察混合溶液颜色的变化_________(填“能”或“不能”)判断反应的先后顺序。
(3)请在下表中写出实验步骤及预期现象和结论:
| 实验步骤 | 预期现象和结论 |
| 取少量反应后的混合溶液分置于A、B两试管中; 往A中滴加__________溶液 往B中滴加__________溶液 | ①若_______________________________ ________________________,则假设1成立 ②若____________________________ ________________________,则假设2成立 ③若______________________________ ______________________,则假设3成立 (4)为了实验成功,必须控制各物质的用量。该小组称取1.52 g FeSO4,同时称取1.66g KI固体,溶于水中。为了验证上述假设,通入的Cl2体积最多不能超过__________L(标准状况)。[相对分子质量:FeSO4 :152??? KI :166 ] [思考与交流] (5)有同学质疑,上述实验只能验证Cl2分别与Fe2+和I-反应的速率大小,并不能证明Fe2+和I-的还原性强弱。于是提出另一方案:往KI溶液中滴入__________溶液,如果能发生反应,即可证明和I-的还原性强于Fe2+。该反应的离子方程式为:____________________ 2、填空题 MnO2一种黑色粉末,既可用于实验室制O2的催化剂,又可以用于实验室制Cl2.某化学实验小组通过实验来探究一黑色粉末是否由MnO2、FeO组成(不含有其它黑色物质).探究过程如下: 3、选择题 从经济效益和环境保护的观点出发,由铜制取硝酸铜最适宜的方法是(????????) 4、计算题 现有表面覆盖铁锈的铁块58.16 g,与足量稀H2SO4反应,可放出22.4 L(标准状况下)H2。反应后溶液中加入KSCN溶液不显红色。求原铁块被氧化的铁的质量。 5、计算题 铁及其化合物在国民经济的发展中起着重要作用。 |