10540
��ijͬѧ����������Ϣ���ƶ�B�ĺ�������Ų���ͼ��ʾ����ͬѧ�����ĵ����Ų�ͼΥ����______��
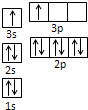
��ACl2������A���ӻ�����Ϊ__________��ACl2�ռ乹��Ϊ__________��
��2����֪C����������Ϊ����ɫ�Ľ��ӡ�������γɵĺϽ����ں�����������䵥��������ǿ���ǿ�D�����ڱ��е縺������Ԫ�ء�E���γɺ�ɫ����ש��ɫ����E2O�ͺ�ɫ��EO��������������������Ϣ��
��д��EԪ��ԭ�ӻ�̬ʱ�ĵ����Ų�ʽ____________________��
����C���ʡ�þ��NaOH��Һ���Թ���ԭ��أ����ĵ缫��ӦʽΪ__________��
��D��Ca2+���γ����ӻ�����侧���ṹ��ͼ��ʾ������Ca2+���ӵ���λ��Ϊ__________�����þ�����ܶ�Ϊag/cm3����þ����������__________cm3��д������ʽ���ɣ���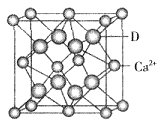
2������� �����������ʵ���Ҫ���������ʽṹ����ش��������⡣
��1����ͼ��ʯī�Ľṹ���侧���д��ڵ���������???????������ţ�
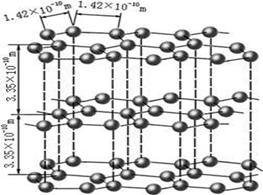
A�Ҽ���B�м���C�����D��λ����E���Ӽ���������F��������G���Ӽ�
��2��������ھ����˵������ȷ����___________
A�������۵��ɵ͵��ߣ�CF4<CCl4<CBr4<CI4
B��Ӳ���ɴ�С�����ʯ>̼����>�����
C���۵��ɸߵ��ͣ�Na>Mg>Al
D���������ɴ�С��NaF> NaCl> NaBr>NaI
��3��CaF2�ṹ��ͼ����ʾ��Cu�γɾ���Ľṹ�����ʾ����ΪH3BO3����ṹͼ(��״�ṹ�����ڵ�H3BO3����ͨ��������)  ?? ??
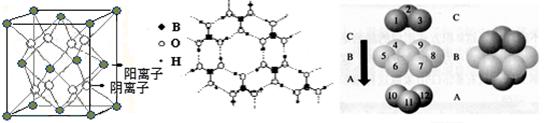
ͼ��?????????????????????????ͼ��????????????????????ͼ��
�� ͼI��ʾ�ľ�������Ca2+��������ҵȾ����Ca2+������Ϊ????????????��
ͼIII��δ��ŵ�Cuԭ���γɾ������Χ����ڵ�Cuԭ����Ϊ??????????????��
��H3BO3������Bԭ���ӻ���ʽ______ ;
�����־������۵�ߵ͵�˳��Ϊ??????????????????(�ѧʽ)��H3BO3���������ۻ�ʱ���˷�����֮��������Ϊ?????????????????
��4�� ̼��ij�ֵ��ʵľ�����ͼ��ʾ��һ����������_____��̼ԭ�ӣ����þ�����ܶ�Ϊ�� g/cm3�������ӵ�������ֵΪNA�����������������̼ԭ��֮��ľ���Ϊ_???____cm(�ô���ʽ��ʾ)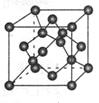
3��ѡ���� ����������ȷ���ǣ�???��
A���Ȼ�菉����У�ÿ1��Cs+������8��Cs+�Ⱦ������
B�����ʯ��״�ṹ�У��ɹ��ۼ����ɵ�̼ԭ�ӻ��У���С�Ļ�����4��̼ԭ��
C��������������ֶѻ�ģ���У��������ܶѻ��������������ܶѻ��Ŀռ����������
D��PCl3����BCl3����������ԭ�ӵ�����㶼�ﵽ8�����ȶ��ṹ
4������� ?����ѧ�D�Dѡ�����ʽṹ�����ʡ���15�֣�
��A��B��C��D��E����Ԫ�ء��������Ϣ���£�

��ش��������⡣
(1) д��EԪ��ԭ�ӻ�̬ʱ�ĵ����Ų�ʽ__________________��
(2) CԪ�صĵ�һ�����ܱ���Ԫ���ĵ�һ������ ______ ______ (���С��)��
(3) CA3������Cԭ�ӵ��ӻ����������____________��
(4) A��C��E����Ԫ�ؿ��γ�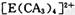 �����ӣ����д��ڵĻ�ѧ�������� ______ (����ţ��� �����ӣ����д��ڵĻ�ѧ�������� ______ (����ţ���
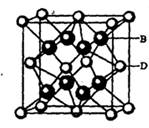
����λ�� �ڽ������ۼ��Թ��ۼ��ܷǼ��Թ��ۼ������Ӽ� �����
��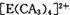 ���жԳƵĿռ乹�ͣ��ҵ� ���жԳƵĿռ乹�ͣ��ҵ�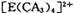 �е�����CA3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ���� �е�����CA3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ���� �Ŀռ乹��Ϊ ____________ (�����)�� �Ŀռ乹��Ϊ ____________ (�����)��
a.ƽ��������b.��������c.������ ?d. V��
(5) B��D���γ����ӻ�����,�侧���ṹ����ͼ��ʾ������D���ӵ���λ��Ϊ_____,���þ�����ܶ�Ϊag ? cm��3,��þ����������______cm-3(д������ʽ����)��
5��ѡ���� ���нṹͼ�У������ǰ������Ԫ�ص�ԭ��ʵ��ԭ��ʵ��ԭ�ӳ�ȥ�������Ӻ�ʣ��IJ��֣���С�ڵ����δ�����γɹ��ۼ����������ӣ����ߴ������ۼ���ʾ����F2 ���ݸ�ͼ��ʾ�Ľṹ�ص㣬�����й�������ȷ���� ���ݸ�ͼ��ʾ�Ľṹ�ص㣬�����й�������ȷ����
 [???? ] [???? ]
A�������ṹͼ�й�����6��Ԫ��
B���ס��ҡ���Ϊ�Ǽ��Է��ӣ���Ϊ���Է���
C�����붡���Է������Ϸ�Ӧ�������ӻ�����
D����CaCl2��Һ�м��루��ͨ�룩���а�ɫ��������
| 
