时间:2017-01-13 09:23:21
1、选择题 下列有关实验操作不正确的是(?????)
A.蒸发时用玻璃棒不断搅拌溶液,待出现较多固体时停止加热
B.将碘水中的碘萃取出来的实验中,萃取剂要求不溶于水,且比水更容易使碘溶解
C.蒸馏操作时,应使温度计水银球插入液态混合物中
D.分液时,打开旋塞,使下层液体流出后,关闭旋塞,上层液体从上口倒出
参考答案:C
本题解析:
试题分析:A.符合蒸发操作的要求,正确。B.萃取实验中,对萃取剂要求是不溶于水,且溶质在其中的溶解度比水更大。正确。C.蒸馏操作时,应使温度计水银球放在蒸馏烧瓶支管口附近。错误。D.符合分液时液体放出原则。正确。
本题难度:一般
2、选择题 下列说法正确的是( )
A.仅用AgNO3溶液便可鉴别亚硝酸钠和食盐
B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大
C.乙酸与乙醇的混合液可用分液漏斗进行分离
D.用标准盐酸滴定待测NaOH溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低
参考答案:B
本题解析:
本题难度:简单
3、实验题 人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+离子,不经处理排放危害极大。某工厂技术人员设计了创新方案,使有害离子的浓度降低到排放标准,同时得到了纯度较高的镍粉。
废液经分析组成如下:
在强酸性的废液中加入NaOH调节pH到2,在搅拌下加入饱和Na2CO3溶液和NaClO除去Mn2+、Co2+,并控制pH不超过3.5(Na2CO3需缓慢加入,防止产生大量CO2而冒槽),过滤后电解含Ni2+的过滤液,以镍铬钛不锈钢片为阴极,以铅片为阳极,电解后在阴极得到镍粉。回答下列问题
⑴ 调节强酸性废液至pH=2,可否直接用饱和Na2CO3溶液?分析你的原因
⑵ 写出除去废液中Mn2+、Co2+的反应方程式
⑶ 搅拌过程中Ni不被沉淀下来,实际操作中是如何实现?
⑷ 电解过程中电流效率与pH的关系如下图,试分析如下图所示变化的原因.并选择电解的最佳pH值
参考答案:⑴ 不可以,将产生大量CO2而冒槽??(1分)
⑵ <
本题解析:⑴认真阅读试题可从题中获得相关信息,当溶液酸性太强时,直接加入饱和Na2CO3溶液会产生大量的CO2,从而发生冒槽。
⑵Mn2+、Co2+在碱性增强的条件下,被ClO-氧化并生成沉淀,通过过滤的方法可以除去这两种杂质离子——这是溶液中除杂最常用的方法之一,如Fe2+的除杂。
Mn2+在碱性条件下,被氧化为+4,以MnO2的形式被除去,离子方程式为: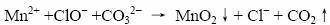
Co2+在碱性条件下不稳定,生成Co(Ⅲ)的氢氧化物,离子方程式如下: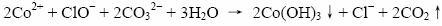
在书写离子方程式的时候,也应该结合题意,溶液由于pH<3.5,仍为酸性条件,所以CO32-结合H+,生成CO2气体。
⑶Ni(Ⅲ)和Co(Ⅲ)都有很强的氧化性,但Ni(Ⅲ)非常不稳定,氧化性比Co(Ⅲ)化合物的氧化性强,因此只要ClO-适量,即使Ni2+被氧化生成了三价镍的化合物,也会被未参加反应的Co2+、Mn2+还原为Ni2+。因此防止Ni2+被沉淀的方法就是控制ClO-的用量。
⑷从图中曲线变化趋势可以看出,当溶液酸性较大时,电解效率很低,随着pH的增大,电解效率增大,但是当pH>4.5后,电解率与溶液pH变化不明显。因此此处要重点分析pH较小时电解效率不高,以及pH较大时电解效率也不高的原因。
由于H+、Ni2+都能在电极的阴极放电,所以当pH较小,也即[H+]较大时,将产生大量的氢气,造成电解效率较低。当pH较大时,由于Ni2+生成了难溶物,溶液中[Ni2+]减小,也造成电解效率低。因此,从图中可以看出来,最佳的pH范围大约为4.0~4.5。
本题难度:一般
4、选择题 下列混合物可用溶解→过滤→蒸发操作分离的是[???? ]
A.混有泥沙的食盐
B.混有水的酒精
C.白糖与食盐的混合物
D.铁粉和泥沙的混合物
参考答案:A
本题解析:
本题难度:简单
5、填空题 (10分)某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程如图(各步反应恰好完全进行)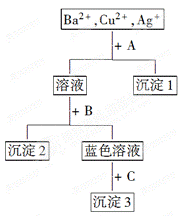
(1)沉淀的化学式:沉淀1__________沉淀2__________沉淀3__________ ;
(2)写出混合液+A的离子方程式:_________?????????????????? ???????????????
???????????????
溶液+B的离子方程式:??????????????????????????????????????
参考答案:(1)AgCl BaSO4 Cu(OH)2
(2)Ag
本题解析:逐一沉淀的要求,要先沉淀出最易形成沉淀的离子,使它不干扰后加试剂的阴离子与其反应,所以沉淀顺序为Ag+―→Cu2+―→Ba2+.
本题难度:一般