时间:2017-01-13 09:09:52
1、填空题 质子核磁共振谱(PMR)是研究有机化合物结构的有力手段之一,在所研究化合物的分子中,每一结构中的等性氢 原子,在PMR谱中都给出了相应的峰(信号),谱中峰的 强度与结构中的氢原子数成正比。例如,乙醛的结构式为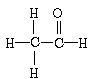 ,其PMR谱中有两个信号,其强度之比为 3:1。
,其PMR谱中有两个信号,其强度之比为 3:1。
(1)化学式为C3H6O2的二元混合物,如果在PMR谱上观察到氢原子给出的峰有两种情况:第一种情况峰的给出强度为3:3,第二种情况峰的给出强度为3:2:1。由此可推断混合物的组成可能是(写结构简式)__________。
(2)在测得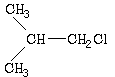 化合物的PMR谱上可观察到三种峰,而测定化合物CH3CH=CHCl时,却得到氢原子给出的信号峰有6种,从原子在空间排列方式不同的角度上,试写出CH3CH=CHCl分子的空间异构体:______________。
化合物的PMR谱上可观察到三种峰,而测定化合物CH3CH=CHCl时,却得到氢原子给出的信号峰有6种,从原子在空间排列方式不同的角度上,试写出CH3CH=CHCl分子的空间异构体:______________。
参考答案:(1)第一种情况是CH3COOCH3 第二种情况是 CH3C
本题解析:
本题难度:一般
2、选择题 对于0.1molH2O,下列说法正确的是
A.含有6.02×1023个H2O分子
B.含0.1molH原子
C.含0.1molO原子
D.含原子总数为0.3
参考答案:C
本题解析:分析:A、每摩尔微粒含有阿伏伽德罗常数个微粒,约为6.02×1023.
B、1个水分子含有2个H原子.
C、1个水分子含有1个O原子.
D、1个水分子含有3个原子(2个H原子、1个O原子).
解答:A、0.1molH2O,约含有6.02×1022个H2O分子,故A错误;
B、1个水分子含有2个H原子,所以0.1molH2O,含0.2molH原子,故B错误;
C、1个水分子含有1个O原子,所以0.1molH2O,含0.1molO原子,故C正确;
D、1个水分 子含有3个原子(2个H原子、1个O原子),所以0.1molH2O,约含原子总数为1.806×1023个原子,故D错误.
故选:C.
点评:考查物质的量相关计算,难度较小,注意基础知识的掌握.
本题难度:一般
3、选择题 能鉴别Na2SO4、Na2SO3、Na2S、Na2CO3四种溶液的一种试剂是
A.AgNO3溶液
B.BaCl2溶液
C.稀硫酸
D.烧碱溶液
参考答案:C
本题解析:分析:四种物质含有的阴离子各不相同,可加入酸进行鉴别,反应现象各不相同.
解答:A.加入AgNO3溶液,都产生沉淀,不能鉴别,故A错误;
B.加入BaCl2溶液,不能鉴别Na2SO4、Na2SO3、Na2CO3,都产生沉淀,故B错误;
C.加入稀硫酸Na2SO4无现象,Na2SO3生成刺激性气体,Na2S生成臭鸡蛋气味的气体,Na2CO3生成无色无味气体,可鉴别,故C正确;
D.加入烧碱溶液,都不反应,不能鉴别,故D错误.
故选C.
点评:本题考查物质的检验和鉴别,题目难度不大,注意把握物质的性质的异同,根据物质的组成特点和性质选择实验方案.
本题难度:简单
4、选择题 同温同压下,下列气体中密度最大的?
A.H2
B.O2
C.N2
D.Cl2
参考答案:D
本题解析:分析:根据ρ=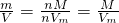 判断;
判断;
解答:ρ=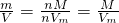 ,同温同压下,气体摩尔体积相同,所以密度与摩尔质量成正比,摩尔质量越大,密度越大,氢气的摩尔质量为2g/mol,氧气的摩尔质量为32g/mol,氮气的摩尔质量为28g/mol,氯气的摩尔质量为71g/mol,摩尔质量最大的是氯气,所以密度最大的是氯气.
,同温同压下,气体摩尔体积相同,所以密度与摩尔质量成正比,摩尔质量越大,密度越大,氢气的摩尔质量为2g/mol,氧气的摩尔质量为32g/mol,氮气的摩尔质量为28g/mol,氯气的摩尔质量为71g/mol,摩尔质量最大的是氯气,所以密度最大的是氯气.
故选D.
点评:本题考查了阿伏伽德罗定律及推论,难度不大,灵活运用有关物质的量的基本公式是解本题的关键.
本题难度:简单
5、选择题 已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是 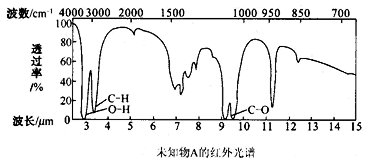
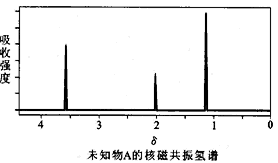
[?????]
A.由红外光谱可知,该有机物中至少含有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3-O-CH3
参考答案:D
本题解析:
本题难度:一般