时间:2017-01-13 08:45:23
1、选择题 2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录.下图中示意的该化合物的晶体结构单元:镁原子间形成正六棱柱,则棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内,则该化合物的化学式可表示为  [???? ]
[???? ]
A.MgB
B.MgB2
C.Mg2B
D.Mg3B2
参考答案:B
本题解析:
本题难度:一般
2、选择题 有四种物质①金刚石 ②白磷 ③甲烷 ④四氯化碳,其中分子具有正四面体构型的是( )
A.①②③
B.①③④
C.②③④
D.①②③④
参考答案:C
本题解析:
本题难度:简单
3、填空题 (1)+3价Co的配合物CoClm・nNH3,中心原子的配位数为6,若1 mol该配合物与足量AgNO3溶液反应生成1 mol AgCl沉淀,用配合物形式写出该配合物的化学式???????????。
(2)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大磁记录性能越好。离子型氧化物MnO2和Fe3O4及Cr2O3中,磁性最大的是___________。
(3)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨(如下左图),每个碳原子通过 ? 杂化与周围碳原子成键。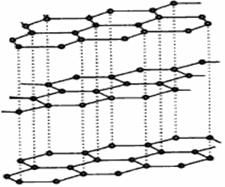 ?
? ?????????????????
?????????????????
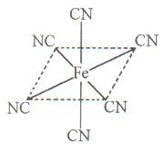
(4)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如上右图。
①已知CN―与N2结构相似,1molCN-中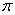 键数目为???????????。
键数目为???????????。
②上述沉淀溶解过程的化学方程式为??????????????????????????????????。
参考答案:(10分)(1)[CoCl2(NH3)4]Cl(2)Fe3O
本题解析:
试题分析:(1)1 mol该配合物与足量AgNO3溶液反应生成1 mol AgCl 沉淀,这说明该配位化合物中有1个氯离子不是配体。又因为Cr是+3价的,则氯原子的购书是3个,由于配位数是6,所以化学式应该是[CoCl2(NH3)4]Cl。
(2)根据核外电子排布式可知,离子型氧化物MnO2和Fe3O4及Cr2O3中金属阳离子含有的未成对电子分别是3、14/3、3,所以磁性最大的Fe3O4。
(3)石墨是层状结构,所以每个碳原子通过sp2杂化与周围碳原子成键。
①CN―与N2结构相
本题难度:一般
4、填空题 (10分)已知有关物质的熔、沸点数据如下表:
| ? | MgO | Al2O3 | MgCl2 | AlCl3 |
| 熔点(℃) | 2852 | 2045 | 714 | 190(2.5×105Pa) |
| 沸点(℃) | 3600 | 2980 | 1412 | 177.8 (1)工业上常用电解熔融MgCl2的方法生产金属镁;用电解Al2O3与冰晶石熔融混合物的方法生产铝。不用电解MgO的方法生产镁的原因是:___▲____; AlCl3可能为___▲____晶体。 (2)请设计可靠的实验证明MgCl2、AlCl3所属化合物的类型,其实验方法是_____▲____ 。 (3)AlCl3具有以下__▲__特殊性质(请填序号)。①液化②挥发③升华 参考答案:共10分 本题解析:略 本题难度:一般 5、选择题 关于化学键的下列说法正确的是????????????????????(???) 参考答案: 本题解析: 本题难度:一般 |