A.1
B.2
C.3
D.5
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列叙述正确的是
[???? ]
A.由极性键结合而成的分子一定是极性分子
B.非极性键只存在于双原子单质分子里
C.非极性分子中,一定含有非极性键
D.一般情况下,极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列分子中划横线的原子采取的杂化方式为 sp杂化的是( )
A.CH4
B.C2H4
C.C2H2
D.NH3
参考答案:C
本题解析:
试题分析:甲烷是正四面体型结构,碳原子是sp3杂化。乙烯是平面型结构,碳原子是sp2杂化。乙炔是直线型结构,碳原子是sp杂化。氨气是三角锥形结构,氮原子含有1对孤对电子,氮原子是sp3杂化,答案选C。
点评:该题是常识性知识的考查,侧重对学生基础知识的巩固,意在培养学生分析问题、解决问题的能力。该题需要在掌握价层电子对互斥理论的基础上,熟练记住常见分子的空间构型特点,有利于培养学生的应试能力,提高学生的学习效率。
本题难度:一般
5、选择题 下列说法中正确的是( )?
A.难失电子的原子,获得电子的能力一定强?
B.易得电子的原子所形成的简单阴离子,其还原性一定强?
C.分子中键能越大,键长越长,则分子越稳定?
D.电子层结构相同的不同离子,核电荷数越多半径越小
参考答案:D?
本题解析:A错误,ⅣA的元素最外层有4个电子,既难失电子,也难获得电子;B错误,易得电子的原子所形成的简单阴离子,其还原性弱;C错误,分子中键能越大,键长越短,分子越稳定;D正确,电子层结构相同的不同离子,核电荷数越多,原子对电子的吸引力越强,半径越小。?
本题难度:一般
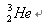 是较为安全的高效核聚变反应原料,
是较为安全的高效核聚变反应原料,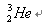 原子核内中子数是( )
原子核内中子数是( )