时间:2017-01-13 08:07:45
1、选择题 下列说法正确的是
A.在气体反应中,升高温度和增大压强都能使单位体积内的反应物中活化分子数和活化分子百分数同时增大
B.pH等于7的溶液一定呈中性
C.c(H+)=c(OH-)的溶液一定呈中性
D.在0.1mol/L的醋酸溶液中,加入少量水平衡向右移,电离平衡常数增大
参考答案:C
本题解析:A错,升高温度,能使单位体积内的反应物中活化分子百分数增大;增大压强,能使单位体积内的反应物中活化分子数增多;
B错,pH等于7的溶液不一定呈中性,如当温度为100℃时,pH=6为中性,而pH=7为碱性。
C正确,任何溶液中,c(H+)=c(OH-)的溶液一定呈中性;
D错,在0.1mol/L的醋酸溶液中,加入少量水平衡向右移,越稀越易电离,电离程度越大,但电离平衡常数不变,电离平衡常数只受温度影响而影响。
本题难度:一般
2、选择题 下列各组数据中,其比值为2:1的是( )
A.相同温度下,0.2mol?L-1乙酸溶液与0.1mol?L-1乙酸溶液中c(H+)之比
B.氨水与(NH4)2SO4溶液混合所得pH=7的溶液中,c(NH+4):c(SO2-4)
C.Na2CO3溶液中,c(Na+):c(CO2-3)
D.pH=12的BA(OH)2溶液与pH=12的KOH溶液中,c[BA(OH)2]:c(KOH)
参考答案:A、弱酸的电离程度规律:越稀越电离,相同温度下,0.2mol
本题解析:
本题难度:一般
3、选择题 下列说法正确的是:( )
A.在100 ℃.101 kPa条件下,液态水的气化热为40.69 kJ・mol-1,则H2O(g) H2O(l) 的ΔH ="+" 40.69 kJ・mol-1
H2O(l) 的ΔH ="+" 40.69 kJ・mol-1
B.已知MgCO3的Ksp = 6.82 × 10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+) = c(CO32-),且c(Mg2+) ・ c(CO32-)= 6.82 × 10-6
C.常温下,在0.10 mol・L-1的NH3・H2O溶液中加入少量NH4Cl晶体,能使NH3・H2O的电离度降低,溶液的pH减小
D.已知:
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ・mol-1 | 348 | 610 | 413 | 436 则可以计算出反应 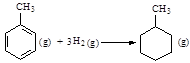 的ΔH为-384 kJ・mol-1 的ΔH为-384 kJ・mol-1 参考答案:C 本题解析: 本题难度:困难 4、简答题 某化学兴趣小组的同学通过实验比较等体积(200mL)0.55mol/L硫酸、1.1mol/L盐酸、1.1mol/L醋酸分别与过量金属反应生成氢气的速率请你协助完成如下实验,并回答相关问题. 参考答案:(1)Na太活泼,能和水反应产生氢气,影响实验结论;Fe与酸 本题解析: 本题难度:一般 5、选择题 下列关于盐酸与醋酸两种稀溶液的说法正确的是(???)? 参考答案:BC 本题解析: 本题难度:一般 |