时间:2017-01-13 07:33:45
1、实验题 某研究性学习小组探究NO3- 在不同环境中的氧化性。
(1)实验一:①试管a、b中均加入等浓度、等体积的NaNO3溶液和等质量的铜片,加热,无明显现象;
②向试管a中加入v mL NaOH溶液,加热,无明显现象;
③向试管b中 加入v mL稀H2SO4,加热,可观察到的现象是_____________。 实验一的目的是__________________。
(2)实验二:利用如图装置探究不同浓度HNO3的氧化性。 
①已知电流计指针偏转方向是电子移动方向。将铜、铁两极同时插入浓HNO3中,观察到电流计指针指向铜,但迅速反转,指针偏向铁一端,此时铁作____(填“正” 或“负”)极;指针反转的原因是____________________。
②将浓HNO3改为稀HNO3后,观察到电流计指针指向铜,此时正极反应式是_________________。
参考答案:(1)③铜溶解,生成无色气体,溶液由无色变蓝色;探究NO3-
本题解析:
本题难度:一般
2、实验题 试用下列试剂:酚酞试液、石蕊试液、稀氨水、氯化铵晶体、浓盐酸、熟石灰粉末、醋酸铵晶体和蒸馏水。根据①弱碱在水中存在电离平衡;②弱碱的阳离子破坏水的电离平衡,这两种平衡移动均会引起指示剂颜色变化,分别选用上述试剂,设计两个实验证明NH3·H2O是弱碱,简述实验方法和现象。 (以离子方程式和简要文字说明)。
参考答案:(1)取少量稀氨水,滴入酚酞试液,溶液呈红色,再加入醋酸铵晶
本题解析:
本题难度:一般
3、实验题 实验题:现有药品:W g(W<1)锌片、稀硫酸、无水硫酸铜、氧化铜和水。请从图中选用适当的实验装置,设计一个简单的实验,粗略测定锌的相对原子质量(假设环境 为标准状况)。
(1)应选用的装置是(只要求写出图中装置的标号)?????????????????????????????????。
(2)所用装置的连接顺序是(填各接口的字母,胶管省略)????????????????????????。
(3)为了保证不漏出氢气,操作中加放试剂 的方法是???????????????????????????。
的方法是???????????????????????????。
(4)用实验所测得的数据,写出计算锌的相对原子质量的数学式:Mr(Zn)=????????。
参考答案:(1)③④⑥
(2)J接 F E接 I
(3)向
本题解析:略
本题难度:简单
4、填空题 (8分)用下图所示的实验过程,测定含Na2SO4的亚硫酸钠中Na2SO3 的质量分数。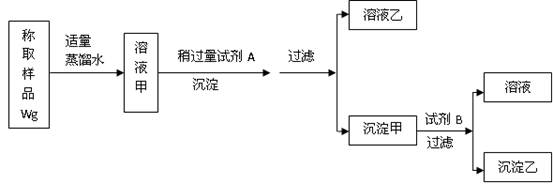
测定沉淀(纯净干燥)的质量W1g,试回答:
(1)试剂A溶液是??????????????????,沉淀乙是???????????????????;
(2)试剂B溶液选用稀盐酸,不能选用稀硝酸的原因是????????????????????????????;
(3)沉淀甲与试剂B反应的离子方程是?????????????????????????????????????????;
(4)计算含Na2SO4的亚硫酸钠中Na2SO3 的质量数???????????????????????????????。
参考答案:(1)BaCl2或Ba(OH)2溶液; BaSO4
(
本题解析:本题重点考察学生对硫酸盐和亚硫酸盐性质的掌握程度。取固体加入蒸馏水之后,获得了Na2SO4和Na2SO3的水溶液,当向其中加入过量A时产生了沉淀,由于高中化学中BaSO4是一种常见的沉淀,学生很容易会想的加入了Ba2+ 所以试剂A中含有Ba2+ ,可以为BaCl2或Ba(OH)2溶液,同时由此可判断沉淀甲为BaSO4和BaSO3的混合物,溶液乙为NaCl,由于加入试剂 B后产生了溶液和沉淀乙,说明沉淀可能部分发生了溶解,结合沉淀物的性质可判断溶剂B为酸,亚硫酸钡溶于酸,而硫酸钡不溶于酸。
(1)试剂A是BaCl2或Ba(OH)2溶液;沉淀乙不溶于试剂B所以沉淀是BaSO4
(2))硝酸具有强氧化性会将亚硫酸钡氧化为硫酸钡,这样无法分离出混合沉淀中原有的硫酸钡,最后无法计算样品中亚硫酸钠的质量分数。
(3)沉淀甲为BaSO4和BaSO3的混合物,当向其中加入酸时会与BaSO3会与酸反应离子反应方程式为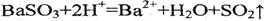
(4)根据反应后剩下沉淀乙硫酸钡的质量计算出其物质的量W1,反应过程中硫酸根离子物质的量守恒可以得出混合物样品中硫酸钠的物质的量,进而求出硫酸钠的质量,用总质量减去硫酸钠的质量即可求出亚硫酸钠的质量,即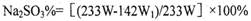
本题难度:一般
5、实验题 用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题: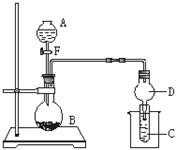
⑴图中D装置在实验中的作用是????????????。
⑵若 A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)?饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程为????????????????????????。
⑶若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现是??????????????????????????????;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的离子反应方程式???????????????????。
⑷若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是??????????????????,C中发生反应的离子方程式为?????????????。
(5)若B为块状大理石,C为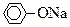 溶液,实验中观察到溶液变浑浊,则酸A不宜用下列的________。
溶液,实验中观察到溶液变浑浊,则酸A不宜用下列的________。
A.HCl
B.HNO3
C.H2SO4
D.CH3COOH
参考答案:本题解析:略
本题难度:一般