时间:2017-01-12 20:07:30
1、填空题 日本核泄漏中最危险的是131I,较大量接触对人体有害,所以不必“谈碘色变”。131?53I在人类生活中还有着“天使”的一面,如控制剂量在医疗上有助于治疗多种甲状腺疾病。在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘。
已知:步骤③中发生的反应是:Fe+2AgI=FeI2+2Ag。
莫尔盐的化学式为:(NH4)2Fe?(SO4)2・6H2O。??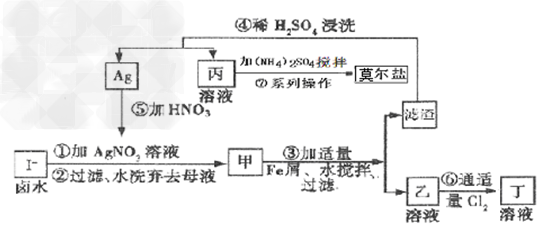
⑴鉴别丙、丁溶液中的金属阳离子可选用的试剂是___________溶液。
⑵步骤④中加入稀H2SO4浸洗的目的是______________。
⑶上述生产流程中,可以循环利用的物质是____________。
⑷“⑦系列操作”包含的操作名称依次为蒸发浓缩、__________、___________、洗涤、干燥。
⑸为了测定富碘卤水中碘离子的含量,可用高锰酸钾滴定法。已知高锰酸钾和碘离子的反应为:2MnO4-+10I-+16H+=2Mn2++5I2+8H2O。
填空:
① 取20.00mL富碘卤水放入__________(填仪器名称)中,将0.1?mol・L-1的酸性高锰酸钾溶液装入滴定管中,达到滴定终点的标志是________________。
② 三次滴定消耗高锰酸钾溶液的部分数据如下表, 
则V3=_____________mL,请根据数据计算富碘卤水中c(I-)=_____________mol・L-1。(精确到0.01)
参考答案:⑴NaOH或KSCN
⑵除去过量的铁屑
⑶Ag<
本题解析:
本题难度:困难
2、填空题 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下: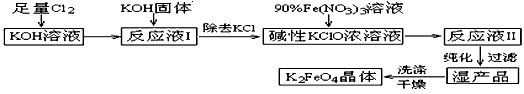
已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH → 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在__________(填“温度较高”或“温度较低”)情况下进行;
(2)写出工业上制取Cl2的化学方程式________________;
(3)K2FeO4具有强氧化性的原因___________________________;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为_________________;
(5)在“反应液I”中加KOH固体的目的是__________________:
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品___________(写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途_______________________________。
参考答案:
(1)温度较低
(2)2NaCl + 2H2O<
本题解析:
本题难度:一般
3、填空题 分析下面两个案例并回答有关问题。
(1)某城镇生产、生活的分布情况如下图所示,河流中W、X、Y、Z处某次水样抽测结果如下表所示。 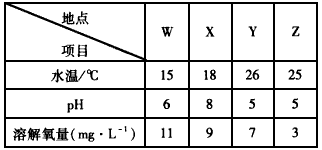

①导致X、Y处水样pH变化的原因可能是__________________,
②Z处鱼类大量减少,产生这种现象的原因可能是________________。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
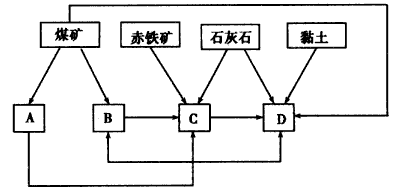
参考答案:(1)①造纸厂排放的碱性污水使X处河水pH升高,火力发电厂净
本题解析:
本题难度:一般
4、填空题 蛇纹石因其花纹似蛇皮而得名,某地蛇纹石大约含MgO38%,另外除了含SiO2外,还含有CaO、Fe2O3、Al2O3等氧化物,由蛇纹石矿制备MgO的工艺流程如下。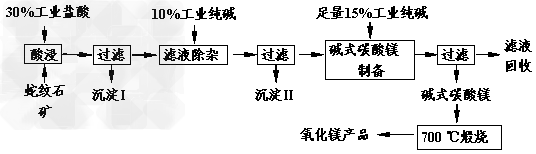
(1)写出酸浸过程中的一个离子方程式_______________。若在实验室进行酸浸过程,需要的仪器有烧杯、__________。
(2)沉淀I的成分是__________(写化学式)。写出它的一个用途___________。
(3)沉淀II的成分是_________________。
(4)从滤液中能回收的物质有____________________。
(5)写出碱式碳酸镁700?℃煅烧产生氧化镁的化学方程式________________?。
参考答案:(1)MgO+2H+=Mg2++H2O(或CaO+2H+=C
本题解析:
本题难度:一般
5、填空题 七水硫酸镁(MgSO4・7H2O)为白色细小四角柱状结晶,无臭,味苦,在干燥空气中易风化,易溶于水,微溶于甘油,微溶于乙醇,热至68℃以上熔化。在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣--硼镁泥可制取七水硫酸镁。
表1 硼镁泥的主要化学成分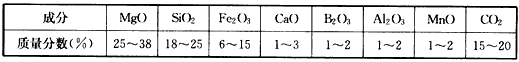
表2 部分阳离子以氢氧化物形式完全沉淀时溶液的pH 
硼镁泥制取七水硫酸镁的工艺流程如下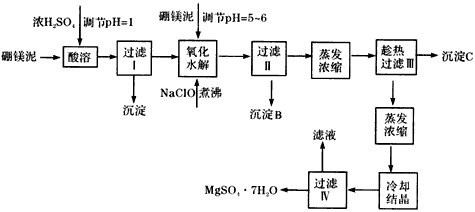
根据以上流程图并参考表格数据,试回答下列问题:
(1)硼镁泥是硼镁矿生产硼砂(Na2B4O7・10H2O)时的废渣。将硼镁矿(2MgO・B2O3)煅烧、粉碎后加水和纯碱,在加热加压下通入CO2可得硼砂。此反应为熵减小反应,试写出反应方程式__________________
(2)沉淀A中除二氧化硅外,还含有硼酸,硼酸微溶于水,为一元弱酸,其酸性不来源于羟基的电离,写出硼酸水溶液电离方程式_____________________
(3)CaSO4的溶解度随温度升高变化不明显,在得到沉淀C时,对蒸发浓缩后的溶液却要进行趁热过滤,原因是______________________
(4)经对沉淀B进行分析,发现其中含有二氧化锰,用化学方程式解释原因:_______________________
(5)用正三辛胺(TOA)做萃取剂,磺化煤油做稀释剂,通过有机萃取也可以用来除去硫酸镁浸出液中的铁。其主要反应如下
Fe3++H2O=Fe(OH)2++H+ (1)
Fe(OH)2++SO42-=Fe(OH)SO4 (2)
2R3N+H2SO4=(R3NH)2SO4 (3)
Fe(OH)SO4+(R3NH)2SO4=Fe(OH)SO4+(R3NH)2SO4 (4)
试问:浸出液初始pH须加H2SO4调至0.9左右,pH>1.5时不利于萃取。试给出须加H2SO4的两个理由
________pH<0.5亦不利于萃取,给出其主要原因_____________________。
参考答案:(1)2MgO・B2O3+Na2CO3+CO2=Na2B4O
本题解析:
本题难度:一般