时间:2017-01-12 19:36:14
1、填空题 (10分)与16g氧气含有相同原子数的氨气(NH3)的质量为???????????;同温同压下,SO2与CO2的密度之比为____________,若质量相同,两种气体的体积比为_________;若体积相同时,两种气体的质量比为______________。水发生电解后所得的混合气体的平均相对分子质量为??????????????
参考答案:4.25g??? 16:11? 11:16? 16:11?
本题解析:考查物质的量的有关计算。
16g氧气的物质的量是16g÷32g/mol=0.5mol。含有的氧原子是0.5mol×2=1mol,所以根据氨气的化学式可知,氨气的物质的量是1mol÷4=0.25mol,质量是0.25mol×17g/mol=4.25g;同温同压下,气体的密度之比是相应的摩尔质量之比,即二者的密度之比是64︰44=16︰11;在质量相等的条件下,SO2和CO2的物质的量之比是44︰64=11︰16,所以二者的体积之比也是11︰16;若体积相等,则在相同条件下,二者的物质的量也是相等的,所
本题难度:一般
2、选择题 浓度为0.01mol·L—1的HCl溶液VmL,加水稀释到2VmL后取出10mL,这10mL溶液中c(H+)为(???)
A.0.05mol/L
B.0.001mol/L
C.0.002mol/L
D.0.005mol/L
参考答案:D
本题解析:略
本题难度:简单
3、选择题 下列溶液中,Cl-的浓度最大的是( )
A.7.5mL2mol/LMgCl2溶液
B.30mL1mol/LKCl溶液
C.10mL3mol/LNaCl溶液
D.30mL0.5mol/LAlCl3溶液
参考答案:A、7.5mL 2mol/LMgCl2溶液中氯离子的物质的量
本题解析:
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA
B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移电子总数为0.2 NA
C.1.8 g重水(D2O)中含NA个中子
D.足量的铜与含2 mol H2SO4的浓硫酸充分反应,可生成NA个SO2分子
参考答案:A
本题解析:
试题分析:A.乙烯和丁烯的最简式是CH2,式量是14,所以室温下,21.0 g乙烯和丁烯的混合气体中含有最简式的物质的量是1.5mol,因此它的碳原子数目为1.5 NA,正确;B.标准状况下,2.24 L Cl2的物质的量是0.1mol,与过量稀NaOH溶液反应,转移电子总数为0.1 NA,错误;C.1.8 g重水(D2O)的物质的量小于0.1mol,因此所含有中子数小于NA个。错误;D.只有浓硫酸能够与Cu反应,所以足量的铜与含2 mol H2SO4的浓硫酸充分反应,生成SO2分子小于NA个。错误;
考点:考查阿伏加德罗常数的计算的知识。
本题难度:一般
5、计算题 有铁和铝的混合物共5.5g,完全溶解于200mL 36.5%的浓盐酸(密度为1.2 g/mL)中,在标准状况下共收集到4.48L H2,求:
(1)浓盐酸的物质的量浓度为??????????。
(2)铁的质量为??????????,铝的质量为??????????。
(3)将反应后剩余的溶液,用水稀释至500mL,求稀释后溶液中盐酸的物质的量浓度(HCl挥发忽略不计)??????????。
参考答案:(1)12mol·L-1(2)2.8g?????2.7g?(
本题解析:
试题分析:(1)根据c=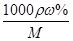 可知
可知
200mL 36.5%的浓盐酸(密度为1.2 g/mL)溶液的物质的量浓度c=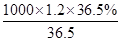 本题难度:简单
本题难度:简单