时间:2017-01-12 17:52:08
1、填空题 (15分)如图所示的装置,X、Y都是惰性电极。将电路接通后,向(乙)中滴人酚酞溶液,在Fe极附近显红色。试回答下列问题: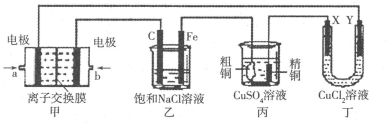
(1)(甲)装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是_______(填“CH4”或“O2”),b处电极上发生的电极反应式是____;
(2)在(乙)装置中,石墨(C)电极上发生_______反应(填“氧化”或“还原”);(乙)装置中总反应的离子方程式是:___________________________________.
(3)如果(丙)装置中精铜电极的质量增加了6.4g,则(乙)装置中,铁电极上产生的气体在标准状况下为____,(甲)装置中消耗的 CH4的质量为____。
(4)(丁)装置中X电极为_______极(填“正”、“负”、“阳”、“阴”),在通电一段时间后,Y电极上发生的电极反应式是_______。
参考答案:(1)CH4O2+2H2O+4e-=4OH-(2)氧化2Cl
本题解析:
试题分析:(1)因为甲为原电池,乙为电解池,因为铁电极附近显红色,说明是溶液中的氢离子放点,铁电极为阴极,则甲中a极为负极,甲烷在负极反应。B为原电池的正极,氧气得到电子生成了氢氧根离子,电极反应为:O2+2H2O+4e-=4OH-。(2)乙中石墨为电解池的阳极,发生氧化反应,乙中是电解氯化钠生成氢氧化钠和氯气和氢气,离子方程式为:2Cl-+2H2O 2OH-+H2↑+Cl2↑。(3)如果精炼铜的电极上质量增加了6.4克,即为0.1摩尔铜,根据电子守恒,所以铁电极上氯离子失去0.2摩尔电子,生成标准状况下氯气的体积为2.24L,则消耗甲烷0.025摩尔,即0.025×16=0.4g。(4)丁中x连接的是原电池的正极,所以为阳极,y为阴极,y极上是溶液中的铜离子得到电子生成铜,电极反应为:Cu2++2e-=Cu。
2OH-+H2↑+Cl2↑。(3)如果精炼铜的电极上质量增加了6.4克,即为0.1摩尔铜,根据电子守恒,所以铁电极上氯离子失去0.2摩尔电子,生成标准状况下氯气的体积为2.24L,则消耗甲烷0.025摩尔,即0.025×16=0.4g。(4)丁中x连接的是原电池的正极,所以为阳极,y为阴极,y极上是溶液中的铜离子得到电子生成铜,电极反应为:Cu2++2e-=Cu。
考点:原电池的原理和电解池的原理的应用。
本题难度:困难
2、选择题 惰性电极电解饱和食盐水,当溶液中有1mol NaOH生成时,则下列说法不正确的是
A.阴极析出氢气
B.标准状况下,阴极产生的气体为11.2L
C.阳极的电极反应式:2H2O + 2e- = 2OH-+ H2↑
D.电路中有1mol电子通过
参考答案:C
本题解析:略
本题难度:简单
3、选择题 下列有关工业生产的叙述正确的是
A.合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率
B.从海水中提镁过程中,电解熔融MgO可制备Mg
C.电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
参考答案:C
本题解析:
试题分析:A、合成氨生产过程中将NH3液化分离,会降低逆反应速率,但不会降低正反应速率,A错误;B、制备Mg应电解熔融MgCl2,B错误;C、电解精炼铜,阳极除了Cu失电子,还有比铜活泼的锌、镍、铁失电子,C正确;D、电解饱和食盐水时用离子交换膜法,防止阳极室产生的Cl2进入阴极室,D错误;答案选C。
考点:考查化学与化工生产。
本题难度:一般
4、填空题 如图为相互串联的甲乙两电解池
试回答:
(1)甲池若为用电解原理精炼铜的装置,则A是??????????????极,材料是?????????????,
电极反应为???????????????????????????????????????????????????。
(2)乙池中若滴入少量酚酞试液,电解一段时间后Fe极附近呈???????????色.
(3)若甲池为电解精炼铜,阴极增重12.8g,则:乙池中阳极放出的气体在标准状况下的体积为
?????????????????????????????????;若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为??????????????????????????。
参考答案:1)阴极;纯铜;Cu2++2 e- =" Cu" ;(2)红
本题解析:
试题分析:结合装置图,与电源负极相连的是阴极,与电源正极相连的是阳极,甲池若为用电解原理精炼铜的装置,则A是阴极,材料为纯铜,发生电极反应是Cu2++2 e- = Cu。
乙池中实质是电解NaCl饱和溶液,C极上放出Cl2,Fe极上生成H2 ,2H2O+2e-=H2↑+2OH,若滴入少量酚酞试液,电解一段时间后Fe极附近呈红色。若甲池为电解精炼铜,阴极增重12.8g,即转移的电子有本题难度:一般
5、选择题 H2O中加入等物质的量的Ag+、Na+、Ba2+、NO3-、SO42-、Cl-,该溶液放在惰性电极的电解槽中通电片刻后,氧化产物与还原产物的质量比是? (??? )????????????
A.1∶8
B.8∶1
C.35.5∶108
D.108∶35.5
参考答案:B
本题解析:在所加入的几种离子中,相互反应生成沉淀的有Ag+和Cl-, Ba2+和SO42-.因为物质的量相同,所以这几种离子全部沉淀完,最后的溶液电解时只相当于电解水,而电解水氧化产物是氧气,还原产物是氢气,两者物质的量为1比2,质量之比为8比1.答案选B
本题难度:一般