时间:2017-01-12 17:45:15
1、填空题 利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下: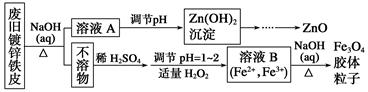
已知:Zn及其化合物的性质与Al及其化合物的性质相似,请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有________。
A.去除油污
B.溶解镀锌层
C.去除铁锈
D.钝化
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是________。
(3)由溶液B制取Fe3O4胶体粒子的过程中,须持续通入N2,其原因是
_______________________________________________________________
(4)Fe3O4胶体粒子能否用减压过滤法实现固液分离?__________(填“能”或“不能”),理由是________________________________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.010 00 mol・L-1的K2Cr2O7标准溶液250 mL,应准确称取________ g K2Cr2O7(保留4位有效数字,已知MK2Cr2O7=294.0 g・mol-1)。配制该标准溶液时,下列仪器中不必要用到的有________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒
⑤容量瓶?⑥胶头滴管 ⑦移液管
(6) 滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”、“偏小”或“不变”)。
参考答案:(1)AB
(2)抽滤、洗涤、灼烧
(3)N2气
本题解析:结合题目提供的信息及制备Fe3O4胶体粒子和ZnO的流程图,运用已有知识分析、解决问题。
(1)由于Zn的性质与Al的相似,可溶于NaOH溶液,因此用NaOH溶液处理废旧镀锌铁皮,除去表面的油污后,可将镀层锌溶解。
(2)调节溶液A的pH产生Zn(OH)2沉淀,然后过滤、洗涤、灼烧使Zn(OH)2分解为ZnO。考虑Zn(OH)2与Al(OH)3的性质相似,应为絮状沉淀物,过滤速度较慢,这里可采用抽滤,加快过滤速度。
(3)溶液B中含有Fe2+、Fe3+,加入NaOH溶液、加热,可得Fe3
本题难度:困难
2、填空题 (13分)Ⅰ、短周期元素X、Y、Z在元素周期表中的相对位置如下图所示。
| | | | X | ||||||
| Y | | | Z 25℃,0.1 mol・L-1M溶液(M为Y的最高价氧化物的水化物)的pH为13。 (1)Y的离子结构示意图为 。 (2)X、Z的气态氢化物稳定性较强的是 (填化学式)。 (3)不能用带磨口玻璃塞的试剂瓶盛装M溶液的原因是 (用离子方程式表示)。 (4)工业上,用X单质制取Z单质的化学方程式为 。 (5)X的最高价氧化物与某一元有机酸的钾盐(化学式为KA,A-为酸根)溶液反应的化学方程式为 。(已知25℃,X的最高价氧化物的水化物的电离常数为Kal =4.2×10-7,Ka2=5.6×10-11;HA的电离常数Ka=1.1×10-10) Ⅱ、碳和氮的化合物与人类生产、生活密切相关。低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。 已知:CO(g) + H2O(g)  H2(g) + CO2(g)的平衡常数随温度的变化如下表: H2(g) + CO2(g)的平衡常数随温度的变化如下表:
|