生成气体的体积/L(标准状况)
| 0.56
| 1.12
| 2.24
实验题 为测定某生铁(假设仅含Fe和C)粉末状样品中铁的质量分数,某化学研究性学习小组设计有关方案进行如下实验。
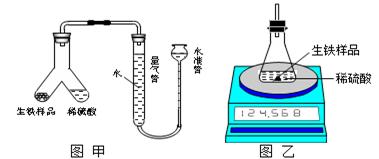
(1)设计如图甲所示装置,使生铁样品与稀硫酸反应的操作为??????????????????????????????????。
实验结束后,读出量气管中的气体体积(换算为标准状况),计算生铁样品中铁的质量分数,测定的结果偏低,可能的原因是???????。(填字母序号)
A. 反应结束并冷却后,未再次调节量气管和水准管中液面相平, 即读取气体体积
B. 稀硫酸过量
C. 水准管中有少量水溢出
(2)设计如图乙所示装置,测得反应前后的有关质量如表,则生铁样品中铁的质量分数为?????????,根据图中装置判断,若实验中操作没有失误,该实验结果可能???????。(填“偏大”、“偏小”或 “准确”)
反应前:整套装置+
稀硫酸质量/g
| 反应前:
生铁样品质量/g
| 反应后:整套装置+
锥形瓶中剩余物的质量/g
| a
| m
| b
(3)若取生铁粉末5.72 g,高温下的氧气流中充分反应,得到CO2气体224 mL(标准状况)。则此生铁粉末中铁和碳的物质的量之比为?????????。若再取三份不同质量的生铁粉末,分别加到100 mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示。计算实验Ⅱ结束后的溶液中,还能溶解生铁样品的质量???????????。
实验序号
| Ⅰ
| Ⅱ
| Ⅲ
| 加入生铁样品的质量/g
| 1.43
| 2.86
| 8.58
| 生成气体的体积/L(标准状况)
| 0.56
| 1.12
| 2.24
本题答案:(10分)(1)将Y型管倾斜,使硫酸溶液流入到生铁样品中。A
本题解析:
试题分析:(1)要使铁样品与稀硫酸反应,就得使铁样品与稀硫酸接触,故操作为将Y型管倾斜,使硫酸溶液流入到生铁样品中。分析结果偏低的原因,A选项中比较合理,故错A。
(2)根据反应后后所得溶液质量=参加反应铁的质量+所加入的稀硫酸的质量-反应放出氢气的质量,计算生铁样品中铁的质量分数为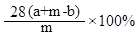 。因为H2会携带水蒸气逸出,故实验结果可能偏大。 。因为H2会携带水蒸气逸出,故实验结果可能偏大。
(3)高温下的氧气流中充分反应,Fe和C都和氧气发生反应,生成CO2气体224 mL(标准状况),即0.01mol,根据化学方程式计算得C的物质的量为0.01mol,质量为0.12g,故生铁的质量为5.72g-0.12g=5.6g,物质的量为0.1mol,故生铁粉末中铁和碳的物质的量之比为0.1mol:0.01mol=10:1。
根据表中数据计算,实验Ⅲ中生铁粉末是过量的,酸反应完,根据生成气体的体积是2.24L计算,酸的物质的量为0.1mol, 实验Ⅱ中酸是过量的,根据根据生成气体的体积是1.1 2L计算,酸反应了0.05mol,剩余0.05mol,故实验Ⅱ结束后的溶液中,还能溶解生铁样品的质量2.86g。
点评:本题主要考查有关化学方程式的计算和化学式的计算,难度较大,根据质量守恒定律,反应后后所得溶液质量=参加反应铁的质量+所加入的稀硫酸的质量-反应放出氢气的质量。
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【一般】
Every man is a fool sometimes,and none at all times. 人都有糊涂的时候,但谁都不会糊涂一生.
|
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|
|
