分装企业
| ?
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
???KIO3+???KI+???H2SO4=???K2SO4+???I2+???H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是?????????????????????????????。
②某学生设计回收四氯化碳的操作步骤为:
a?将碘的四氯化碳溶液置于分液漏斗中;
b?加入适量;
c?分离出下层液体。
以 www.91exAm.org上设计中遗漏的操作及在上述步骤中的位置是??????????????????????。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a?准确称取wg食盐,加适量蒸馏水使其完全溶解;
b?用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c?以淀粉为指示剂,逐滴加入物质的量浓度为1.00×10-3mol・L-1的Na2S2O3溶液24.00mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是?????????????????????。
②b中反应所产生的I2的物质的量是?????????mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)????mg/kg。
实验题 (12分)目前市场来源:91考试网 www.91eXam.org销售的某种食用精制盐包装袋上有如下说明:
产品标准
| GB5461
| 产品等级
| 一级
| 配料
| 食盐、碘酸钾、抗结剂
| 碘含量(以I计)
| 20~50mg/kg
| 分装日期
| ?
| 分装企业
| ?
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
???KIO3+???KI+???H2SO4=???K2SO4+???I2+???H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是?????????????????????????????。
②某学生设计回收四氯化碳的操作步骤为:
a?将碘的四氯化碳溶液置于分液漏斗中;
b?加入适量;
c?分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是??????????????????????。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a?准确称取wg食盐,加适量蒸馏水使其完全溶解;
b?用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c?以淀粉为指示剂,逐滴加入物质的量浓度为1.00×10-3mol・L-1的Na2S2O3溶液24.00mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是?????????????????????。
②b中反应所产生的I2的物质的量是?????????mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)????mg/kg。
本题答案:(1)1、5、3、3、3、3
(2)①I2+SO32-
本题解析:
试题分析:(1)根据化合价升降法配平方程式为KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(2)①Na2SO3溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+。
②回收CCl4的时候,加入Na2SO3溶液后,要振荡静置,然后才能分液,所以在步骤b后,增加操作:将分液漏斗充分振荡后静置。
(3)①以淀粉做指示剂的时候,当I2反应完后,恰好完全反应,所以溶液由蓝色变为无色。
②反应后生成I2的物质的量为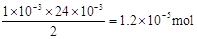 。 。
精制盐的含碘量为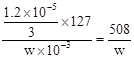
点评:本题很基础,主要考查学生的计算能力和分析问题的能力。
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【一般】
As you make your bed so you must lie on it. 自己铺的床必须自己去躺。/ 自作则自受。
|
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|