时间:2017-01-05 11:08:01
实验题 (1)?利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
Ni(s)+4CO(g)?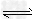 Ni(CO)4(g)?该反应的ΔH_________0?(选填“>”或“=”或“<”)。
Ni(CO)4(g)?该反应的ΔH_________0?(选填“>”或“=”或“<”)。
(2)?在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g)??????????ΔH1=-393.5?kJ・mol-1
CO2(g)+C(s)=2CO(g)????????ΔH2=+?172.5?kJ・mol-1
S(s)+O2(g)=SO2(g)??????????ΔH3=-296.?0?kJ・mol-1
请写出CO除SO2的热?化学方程式__________。
(3)?已知Na2CrO4溶液酸化时发生的反应为:2CrO42-+2H+?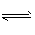 Cr2O72-+H2O,若1L酸化后所得溶液中铬元素的总?物质的量为0.55?mol,CrO42-有10/11转化为Cr2O72-。又知:常温时该反应的平衡常数K=1014。求上述酸化后所得溶?液的pH_________。
Cr2O72-+H2O,若1L酸化后所得溶液中铬元素的总?物质的量为0.55?mol,CrO42-有10/11转化为Cr2O72-。又知:常温时该反应的平衡常数K=1014。求上述酸化后所得溶?液的pH_________。
(4)?根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7?mol・L-1以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①?沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于_________mol・L-1,然后再进行后续?处理方能达到国家排放?标准。若原废水中CrO42-浓度为a?mol/L,请在图中画出c(CrO42-)与c(Ba2+)的关系图,并进行必要的标注。 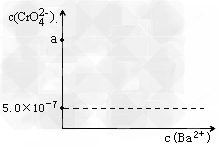
②?还原法:CrO42-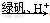 Cr3+
Cr3+ Cr(OH)3。用该方法处理10?m3?CrO42-的物质的量浓度为1.0×10-3?mol・L-1的来源:91考试网 91exam.org废水,至少需要绿矾(FeSO4・7H2O,相对分子质量为278)__________Kg(保留两位小数)。
Cr(OH)3。用该方法处理10?m3?CrO42-的物质的量浓度为1.0×10-3?mol・L-1的来源:91考试网 91exam.org废水,至少需要绿矾(FeSO4・7H2O,相对分子质量为278)__________Kg(保留两位小数)。
实验题 (1)?利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
Ni(s)+4CO(g)?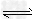 Ni(CO)4(g)?该反应的ΔH_________0?(选填“>”或“=”或“<”)。
Ni(CO)4(g)?该反应的ΔH_________0?(选填“>”或“=”或“<”)。
(2)?在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g)??????????ΔH1=-393.5?kJ・mol-1
CO2(g)+C(s)=2CO(g)????????ΔH2=+?172.5?kJ・mol-1
S(s)+O2(g)=SO2(g)??????????ΔH3=-296.?0?kJ・mol-1
请写出CO除SO2的热?化学方程式__________。
(3)?已知Na2CrO4溶液酸化时发生的反应为:2CrO42-+2H+?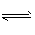 Cr2O72-+H2O,若1L酸化后所得溶液中铬元素的总?物质的量为0.55?mol,CrO42-有10/11转化为Cr2O72-。又知:常温时该反应的平衡常数K=1014。求上述酸化后所得溶?液的pH_________。
Cr2O72-+H2O,若1L酸化后所得溶液中铬元素的总?物质的量为0.55?mol,CrO42-有10/11转化为Cr2O72-。又知:常温时该反应的平衡常数K=1014。求上述酸化后所得溶?液的pH_________。
(4)?根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7?mol・L-1以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①?沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于_________mol・L-1,然后再进行后续?处理方能达到国家排放?标准。若原废水中CrO42-浓度为a?mol/L,请在图中画出c(CrO42-)与c(Ba2+)的关系图,并进行必要的标注。 
②?还原法:CrO42-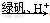 Cr3+
Cr3+ Cr(OH)3。用该方法处理1 91exam .org0?m3?CrO42-的物质的量浓度为1.0×10-3?mol・L-1的废水,至少需要绿矾(FeSO4・7H2O,相对分子质量为278)__________Kg(保留两位小数)。
Cr(OH)3。用该方法处理1 91exam .org0?m3?CrO42-的物质的量浓度为1.0×10-3?mol・L-1的废水,至少需要绿矾(FeSO4・7H2O,相对分子质量为278)__________Kg(保留两位小数)。
本题答案:(1)<
(2)2CO(g)+SO2(g)=S(s)+
本题解析:
本题所属考点:【氧化还原、电化学的计算】
本题难易程度:【一般】