时间:2017-01-04 15:59:33
选择题 铁的氧化物可用于脱除煤气中的H2S,该反应原理为:
①Fe3O4 (s)+3H2S(g)+H2 (g) 3FcS(s)+4H2O(g)??△H=a kJ ? mol-1
3FcS(s)+4H2O(g)??△H=a kJ ? mol-1
②Fe2O3(s)+2H2S(g) + H2(g) 2FeS(s)+3H2O(g)?△H=bkJ ? mol-1
2FeS(s)+3H2O(g)?△H=bkJ ? mol-1
③FeO(s)+H2S(g)  FeS(s)+H2O(g) ?△H=ckJ・ mol-1
FeS(s)+H2O(g) ?△H=ckJ・ mol-1
温度与平衡常数的关系如图,下列有关说法正确的是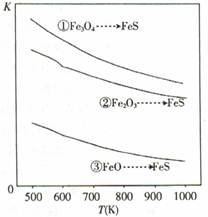
A.a、b、c均小于0
B.压强越大,H2S的脱除率越高
C.温度越高,H2S的脱除率越高
D.反应①、②、③的平衡常数表达式相同
选择题 铁的氧化物可用于脱除煤气中的H2S,该反应原理为:
①Fe3O4 (s)+3H2S(g)+H2 (g) 3FcS(s)+4H2O(g)??△H=a kJ ? mol-1
3FcS(s)+4H2O(g)??△H=a kJ ? mol-1
②Fe2O3(s)+2H2S(g) + H2(g) 2FeS(s)+3H2O(g)?△H=bkJ ? mol-1
2FeS(s)+3H2O(g)?△H=bkJ ? mol-1
③FeO(s)+H2S(g)  FeS(s)+H2O(g) ?△H=ckJ・ mol-1
FeS(s)+H2O(g) ?△H=ckJ・ mol-1
温度与平衡常数的关系如图,下列有关说法正确的是
A.a、b、c均小于0
B.压强越大,H2S的脱除率越高
C.温度越高,H2S的脱除率越高
D.反应①、②、③的平衡常数表达式相同
本题答案:A
本题解析:
试题分析:从图像可知,升高温度。三个反应的平衡常数都减小,说明平衡都向逆反应方向移动,逆反应吸热,正反应放热,故a、b、c均小于0,A正确;反应①、②是气体分子总数增加反应,增大压强平衡逆向移动,H2S的脱除率降低,B错;升高温度,平衡逆向移动,H2S的脱除率降低,C错;因三个反应中气体的化学计量数不同,因此平衡常数的表达式不同,D错。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】