时间:2016-12-31 17:39:41
填空 题 工业上利用硅的氧化物制取硅单质,主要反应为:SiO2 + 2C 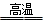 Si + 2CO↑。该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为 mol。
Si + 2CO↑。该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为 mol。
填空题 工业上利用硅的氧化物制取硅单质,主要反应为:SiO2 + 2C 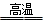 Si + 2CO↑。该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为 mol。
Si + 2CO↑。该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为 mol。
本题答案:C SiO2
本题解析:
试题分析:SiO2 + 2C 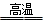 Si + 2CO↑中,SiO2→Si化合价由+4价变成了0价,化合价降低是氧化剂,被还原,被还原的物质是SiO2;C→CO化合价由0价变成+2价,化合价升高是还原剂,被氧化,还原剂是SiO2;1molC参加本反应,共转移2mole-,2molC参加反应转移4mole-,根据化学反应方程式,2molC参加反应共生成1molSi。
Si + 2CO↑中,SiO2→Si化合价由+4价变成了0价,化合价降低是氧化剂,被还原,被还原的物质是SiO2;C→CO化合价由0价变成+2价,化合价升高是还原剂,被氧化,还原剂是SiO2;1molC参加本反应,共转移2mole-,2molC参加反应转移4mole-,根据化学反应方程式,2molC参加反应共生成1molSi。
考点:考查氧化还原反应的定义及转移电子数等相关知识。
本题所属考点:【化学基本概念】
本题难易程度:【一般】