时间:2016-12-26 22:58:45
简答题 (14分)用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
(1) SiCl4的平均反应速率为___
(2)平衡后,若改变温度,混合气体的平均相对分子质量与温度的关系如图所示,下列说法正确的是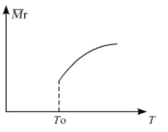
A.该反应在任何温度下可自发进行
B.若混合气体的总质量不变,表明上述反应己达到平衡状态
C.其他条件不变,增大Si3N4的物质的量,平衡向左移动
D.按3:2:6的物质的量比增加反应物,SiC14(g)的转化率降低
(3)下表为不同温度下该反应的平衡常数,其他条件相同时,在来源:91考试 网___(填"T1”、“T2”.,“T3”)温度下反应达到平衡所需时间最长:
假设温度为T1时向该反应容器中同时加入。(SiC14) =0.3 mol/L,c(H2) =0.3 mol/L,,c(N2) =
x mol/L, c (HCl) =0.3 mol/L和足量Si3N4 (s),若要使平衡建立的过程中HCl浓度减小,x的取值
范围为___
(4)该反应的原子利用率为____
(5)工业上制备SiCl4的反应过程如下: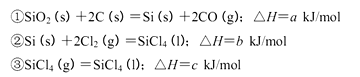
写出二氧化硅、焦炭与Cl 2在高温下反应生成气态SiC14和一氧化碳的热化学方程式_____
简答题 (14分)用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
(1) SiCl4的平均反应速率为___
(2)平衡后,若改变温度,混合气体的平均相对分子质量与温度的关系如图所示,下列说法正确的是
A.该反应在任何温度下可自发进行
B.若混合气体的总质量不变,表明上述反应己达到平衡状态
C.其他条件不变,增大Si3N4的物质的量,平衡向左移动
D.按3:2:6的物质的量比增加反应物,SiC14(g)的转化率降低
(3)下表为不同温度下该反应的平衡常数,其他条件相同时,在___(填"T1”、“T2”.,“T3”)温度下反应达到平衡所需时间最长:
假设温度为T1时向该反应容器中同时加入。(SiC14) =0.3 mol/L,c(H2) =0.3 mol/L,,c(N2) =
x mol/L, c (HCl) =0.3 mol/L和足量Si3N4 (s),若要使平衡建立的过程中HCl浓度减小,x的取值
范围为___
(4)该反应的原子利用率为____
(5)工业上制备SiCl4的反应过程如下: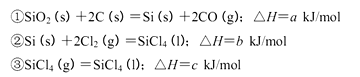
写出二氧化硅、焦炭与Cl 2在高温下反应生成气态SiC14和一氧化碳的热化学方程式_____
本题答案:(14分)
(1)0.015mol/(L?min)(2
本题解析:
试题分析:(1)反应生成的n(Si3N4)=2.8g÷140g/mol=0.02mol,则反应的SiCl4为:n(SiCl4)=3n(Si3N4)=3×0.02mol=0.06mol,则v(Si3N4)=0.06mol÷2L÷2min=0.015mol/(L?m来源:91考试网 91Exam.orgin)。
(2)正反应方向,气体的物质的量增大,气体的质量减小,根据图像可知温度升高,混合气体的平均相对分子质量增大,所以升温平衡向逆反应方向移动移动,则该反应为放热反应。A、因为该反应?H <0,?S>0,所以?H?―T?S恒小于0,在任何温度下可自发进行,正确;B、因为Si3N4为固体,反应前后气体的质量不相等,所以若混合气体的总质量不变,表明反应己达到平衡状态,正确;C、因为Si3N4为固体,所以其他条件不变,增大Si3N4的物质的量,对平衡无影响,错误;D、按3:2:6的物质的量比增加反应物,H2的体积分数增大,所以SiC14(g)的转化率增大,错误。
(3)该反应为放热反应,随着温度升高,平衡常数减小,所以T3温度最低,反应速率最小,达到平衡所需时间最长;当反应恰好达到平衡时,根据平衡常数可得:0.312÷(0.33×0.36×x2)=1.2,解得x=0.15mol,要使平衡建立的过程中HCl浓度减小,反应向左进行,所以0 ≤ x < 0.15
(4)根据化学方程式,原子的利用率=140÷(140+12×36.5)×100%=24.22%
(5)首先写出化学方程式并注明状态:SiO2(s)+2C(s)+2Cl2(g)=SiCl4(g)+2CO(g),然后根据盖斯定律求算焓变,该反应可由已知的3个反应经① + ②―③求得,所以?H=(a+b-c)kJ?mol?1,进而可写成化学方程式。
考点:本题考查化学反应速率、化学平衡、原子利用率、热化学方程式的书写。
本题所属考点:【热化学方程式】
本题难易程度:【一般】