填空题 (本题共12分)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的。汽车尾气脱硝脱碳的主要原理为:
2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=  Q(Q>0)。
Q(Q>0)。
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s
| 0
| 1
| 2
| 3
| 4
| 5
|
c(NO)/mol・L-1
| 1.00×10-3
| 4.50×10-4
| 2.50×10-4
| 1.50×10-4
| 1.00×10-4
| 1.00×10-4
|
c(CO)/mol・L-1
| 3.60×10-3
| 3.05×10-3
| 2.85×10-3
| 2.75×10-3
| 2.70×10-3
| 2.70×10-3
|
29.写出该反应的平衡常数表达式__________________________________________。
30.前2s内的平均反应速率υ(N2) =
mol/(L・s);达到平衡时,CO的转化率为
。
31.下列描述中能说明上述反应已达平衡的是________________
A.2υ正(NO)=υ逆(N2)
B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中CO的转化率不再发生变化
32.采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液。往(NH4)2SO4溶液中再加入少量(NH4)2SO4固体,
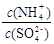
的值将
(填“变大”、“不变”或“变小”)
33.有物质的量浓度相等的三种铵盐溶液:①NH4Cl ②NH4HCO3 ③NH4HSO4,这三种溶液中水的电离程度由大到小的顺序是________________(填编号);
34.向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀。用电离平衡原理解释上述现象__________________________________________________________。
填空题 (本题共12分)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的。汽车尾气脱硝脱碳的主要原理为:
2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=  Q(Q>0)。
Q(Q>0)。
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s
| 0
| 1
| 2
| 3
| 4
| 5
|
c(NO)/mol・L-1
| 1.00×10-3
| 4.50×10-4
| 2.50×10-4
| 1.50×10-4
| 1.00×10-4
| 1.00×10-4
|
c(CO)/mol・L-1
| 3.60×10-3
| 3.05×10-3
| 2.85×10-3
| 2.75×10-3
| 2.70×10-3
| 2.70×10-3
|
29.写出该反应的平衡常数表达式__________________________________________。
30.前2s内的平均反应速率υ(N2) =
mol/(L・s);达到平衡时,CO的转化率为
。
31.下列描述中能说明上述反应已达平衡的是________________
A.2υ正(NO)=υ逆(N2)
B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中CO的转化率不再发生变化
32.采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液。往(NH4)2SO4溶液中再加入少量(NH4)2SO4固体,
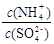
的值将
(填“变大”、“不变”或“变小”)
33.有物质的量浓度相等的三种铵盐溶液:①NH4Cl ②NH4HCO3 ③NH4HSO4,这三种溶液中水的电离程度由大到小的顺序是________________(填编号);
34.向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀。用电离平衡原理解释上述现象__________________________________________________________。
本题答案:29.K=c(N2)・c(CO2) 2/c(NO)2・c(C
本题解析:
试题分析:29.反应2NO(g)+2CO(g)
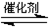
N2(g)+2CO2(g)的化学平衡常数是K=c(N2)・c(CO2) 2/c(NO)2・c(CO)2;
30. 在前2s内,c(NO)由1.00×10-3mol/L变为2.50×10-4mol/L,改变了7.50×10-4mol/L,则根据方程式中NO与N2的反应关系可知N2浓度是7.50×10-4mol/L÷2=3.75mol/L。则V(N2)= 3.75mol/L÷2s=1.875×10-4 mol/(L・s);达到平衡时,CO的转化率为[(3.60×10-3mol/L-2.70×10-3mol/L)÷3.60×10-3mol/L]×100%=25%;
31. A.在任何时刻都存在:υ正(NO)=2υ正(N2) 。若2υ正(NO)=υ逆(N2),则υ逆(N2)=4υ正(N2) ,用同一种物质表示的化学反应速率,正逆反应速率不等,反应没有处于平衡状态,错误; B.由于该反应是反应前后气体体积不等的质量不变的反应,若反应达到平衡状态,则气体的物质的量不变,容器中气体的平均分子量就不变,因此容器中气体的平均分子量应不随时间而变可以证明反应处于平衡状态,正确;C.由于该反应反应物和生成物都是气体,容器的容积不变,所以在任何时刻容器中气体的密度都不会发生变化,因此不能作为判断平衡的标志,错误; D.若容器中CO的物质的量发生变化,反应就没有达到平衡状态,若达到平衡状态,则CO的物质的量不变,CO的转化率不变,反应处于平衡状态,正确;
32.往(NH4)2SO4的稀溶液中再加入少量(NH4)2SO4固体,溶液的浓度增大。由于该盐是强酸弱碱盐,NH4+会发生水解反应而消耗,浓度增大,盐的水解平衡逆向移动,盐水解的程度减小,
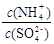
的值将变大。
33.在三种盐溶液中都存在NH4+的水解作用,NH4++H2O
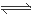
NH3・H2O+H+;NH4+水解使溶液显酸性,在NH4HCO3溶液中除了存在NH4+水解外,还存在HCO3-的水解作用:HCO3-+H2O
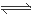
H2CO3+OH-;HCO3-水解使溶液显碱性,二者的水解的酸碱性相反,对彼此的水解起促进作用,所以水解程度增大。对于NH4HSO4来说,是强酸的酸式盐,NH4HSO4=NH4++H++SO42-。电离产生的H+对NH4+的水解平衡起抑制作用,是其水解程度减小。所以① NH4Cl、②NH4HCO3、③NH4HSO4这三种溶液中水的电离程度由大到小的顺序是②>①>③;
34.由于酸性HCl>H2SO3,所以向BaCl2溶液中通入足量SO2气体,只发生化合反应:SO2+H2O= H2SO3,H2SO3是弱酸,电离产生的SO32-浓度很小,没有发生复分解反应生成沉淀生成,继续滴加一定量的氨水后,氨水电离产生的OH-对H2SO3的电离平衡起促进作用,产生更多的SO32-,使c(SO32-)增大,SO32-就与溶液中的Ba2+结合生成BaSO3沉淀。
考点:考查化学平衡常数的表达式的书写、化学平衡状态的判断、盐的水解程度的大小比较及影响因素、程度平衡理论的应用、化学反应速率和物质的平衡转化率的计算的知识。
本题所属考点:【盐类水解的原理】
本题难易程度:【困难】
A thing you don't want is dear at any price. 不需要的东西,无论买价多少都贵.
 N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=  Q(Q>0)。
Q(Q>0)。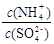 的值将 (填“变大”、“不变”或“变小”)
的值将 (填“变大”、“不变”或“变小”) N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=  Q(Q>0)。
Q(Q>0)。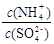 的值将 (填“变大”、“不变”或“变小”)
的值将 (填“变大”、“不变”或“变小”)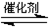 N2(g)+2CO2(g)的化学平衡常数是K=c(N2)・c(CO2) 2/c(NO)2・c(CO)2;
N2(g)+2CO2(g)的化学平衡常数是K=c(N2)・c(CO2) 2/c(NO)2・c(CO)2;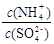 的值将变大。
的值将变大。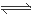 NH3・H2O+H+;NH4+水解使溶液显酸性,在NH4HCO3溶液中除了存在NH4+水解外,还存在HCO3-的水解作用:HCO3-+H2O
NH3・H2O+H+;NH4+水解使溶液显酸性,在NH4HCO3溶液中除了存在NH4+水解外,还存在HCO3-的水解作用:HCO3-+H2O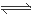 H2CO3+OH-;HCO3-水解使溶液显碱性,二者的水解的酸碱性相反,对彼此的水解起促进作用,所以水解程度增大。对于NH4HSO4来说,是强酸的酸式盐,NH4HSO4=NH4++H++SO42-。电离产生的H+对NH4+的水解平衡起抑制作用,是其水解程度减小。所以① NH4Cl、②NH4HCO3、③NH4HSO4这三种溶液中水的电离程度由大到小的顺序是②>①>③;
H2CO3+OH-;HCO3-水解使溶液显碱性,二者的水解的酸碱性相反,对彼此的水解起促进作用,所以水解程度增大。对于NH4HSO4来说,是强酸的酸式盐,NH4HSO4=NH4++H++SO42-。电离产生的H+对NH4+的水解平衡起抑制作用,是其水解程度减小。所以① NH4Cl、②NH4HCO3、③NH4HSO4这三种溶液中水的电离程度由大到小的顺序是②>①>③;