ЪБМф:2016-12-25 15:58:28
бЁдёЬт 25CЪБЃЌгУХЈЖШЮЊ0.1000 mol/LЕФNaOHШмвКЕЮЖЈ20. 00 mL 0 .1000 molЁЄL-1ЕФ
CH3COOH.ЁЃЕЮЖЈЧњЯпШчЭМЫљЪОЁЃЯТСаЗжЮіДэЮѓЕФЪЧ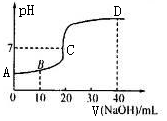
AЃЎCЕуЕФШмвКЃКcЃЈCH3COOвЛЃЉ+c(CH.3COOH)>c(Na+)
BЃЎBЕуЕФШмвКc (CH3COOвЛ)>c(Na+ЃЉ>c(H+ЃЉ> c(OH-)
CЃЎAЕуЕФзнзјБъжЕЮЊl
DЃЎDЕуШмвК2c(CH3 COOH)ЪЎc(H+) =c(OHЁЊ)ЁЊc(CH3COOЁЊ)
бЁдёЬт 25CЪБЃЌгУХЈЖШЮЊ0.1000 mol/LЕФNaOHШмвКЕЮЖЈ20. 00 mL 0 .1000 molЁЄL-1ЕФ
CH3COOH.ЁЃЕЮЖЈЧњЯпШчЭМЫљЪОЁЃЯТСаЗжЮіДэЮѓЕФЪЧ
AЃЎCЕуЕФШмвКЃКcЃЈCH3COOвЛЃЉ+c(CH.3COOH)>c(Na+)
BЃЎ BЕуЕФШмвКc (CH3COOвЛ)>c(Na+ЃЉ>c(H+ЃЉ> c(OH-)
CЃЎAЕуЕФзнзјБъжЕЮЊl
DЃЎDЕуШмвК2c(CH3COOH)ЪЎc(H+) =c(OHЁЊ)ЁЊc(CH3COOЁЊ)
БОЬтД№АИЃКC
БОЬтНтЮіЃК
ЪдЬтЗжЮіЃКAЁЂCЕуЪБШмвКЮЊжаадЃЌЫљвдcЃЈCH3COOвЛЃЉ= c(Na+),ЫљвдcЃЈCH3COOвЛЃЉ+c(CH.3COO)H>c(Na+)ЃЌе§ШЗЃЛBЁЂBЕуБэЪОДзЫсгыЧтбѕЛЏФЦЮДЭъШЋЗДгІЃЌДЫЪБЮЊДзЫсгыДзЫсФЦЕФЛьКЯвКЃЌШмвКЯдЫсадЃЌЫљвдc (CH3COOвЛ)>c(Na+ЃЉ>c(H+ЃЉ> c(OH-)ЃЌе§ШЗЃЛCЁЂAЕуБэЪОДзЫсШмвКЕФpHЃЌДзЫсЪЧШѕЫсЃЌЫљвдХЈЖШЪЧ0.1000mol/LЕФДзЫсШмвКЕФpHДѓгк1ЃЌДэЮѓЃЛDЁЂDЕуБэЪОЕШХЈЖШЕФЧтбѕЛЏФЦгыДзЫсФЦЕФЛьКЯвКЃЌЫљвдгаc(Na+)=2ЃЈcЃЈCH3COOвЛЃЉ+c(CH.3COOH)ЃЉЃЌИљОнЕчКЩЪиКуПЩЕУcЃЈCH3COOвЛЃЉ+ c(OHЁЊ)= c(Na+)+ c(H+)ЃЌСНЪНСЊСЂПЩЕУ2c(CH3COOH)ЪЎc(H+) =c(OHЁЊ)ЁЊc(CH3COOЁЊ)ЃЌе§ШЗЃЌД№АИбЁCЁЃ
ПМЕуЃКПМВщЖдЕчНтжЪШмвКЕФХаЖЯЃЌРызгХЈЖШЕФБШНЯЃЌЪиКуЙцТЩЕФгІгУ
БОЬтЫљЪєПМЕуЃКЁОбЮРрЫЎНтЕФдРэЁП
БОЬтФбвзГЬЖШЃКЁОвЛАуЁП