时间:2016-12-24 00:32:34
选择题 已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黄色)=1.2×10-14。如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-==CuCl。下列说法不正确的是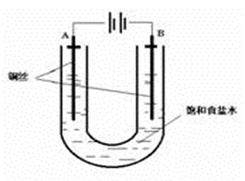
A.B极发生的电极反应为2H++2e-==H2↑
B.实验开始时 ,A极附近出现白色浑浊
C.电解时,Na+移向A极
D.一段时间后,U形管底部形成橙黄色沉淀
选择题 已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黄色)=1.2×10-14。如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-==CuCl。下列说法不正确的是
A.B极发生的电极反应为2H++2e-==H2↑
B.实验开始时,A极附近出现白色浑浊
C.电解时,Na+移向A极
D.一段时间后,U形管底部形成橙黄色沉淀
本题答案:C
本题解析:
试题分析:B为阴极,发生还原反应,电极方程式为2H++2e-=H2↑,A正确;铜为阳极,发生氧化反应,电极反应为Cu-e-+Cl-=CuCl,可观察到A极附近出现白色浑浊,B正确;电解时,阳离子向阴极移动,即移向B极,C错误;.因Kap(CuOH)<Kap (CuCl),则可生成CuOH橙黄色沉淀,D正确.
考点:考查原电池和电解池的工作原理。
本题所属考点:【电解池原理】
本题难易程度:【一般】