时间:2016-12-18 16:49:27
选择题 已知0.5L盐酸和硫酸的混合溶液中含有0.1mol?Cl-和0.2mol?SO42-,则此溶液中H+的物质的量浓度是
A.1?mol/L
B.0.5?mol/L
C.0.6?mol/L
D.0.1?mol/L
选择题 已知0.5L盐酸和硫酸的混合溶液中含有0.1mol?Cl-和0.2mol?SO42-,则此溶液中H+的物质的量浓度是
A.1?mol/L
B.0.5?mol/L
C.0.6?mol/L
D.0.1?mol/L
本题答案:A
本题解析:分析:根据电荷守恒溶液中n(H+)=n(Cl-)+2n(SO42-),再根据c=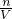 计算氢离子的浓度.
计算氢离子的浓度.
解答:0.5L盐酸和硫酸的混合溶液中含有0.1mol?Cl-和0.2mol?SO42-,
根据电荷守恒溶液中n(H+)=n(Cl-)+2n(SO42-)=0.1mol+2×0.2mol=0.5mol,
故溶液中氢离子的浓度为: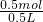 =1mol/L,
=1mol/L,
故选A.
点评:本题考查物质的量浓度的有关计算,难度不大,注意电解质混合溶液中利用电荷守恒进行的计算.
本题所属考点:【化学实验】
本题难易程度:【简单】