时间:2016-12-18 14:51:28
选择题 取不同质量的镁铝合金分别与25mL同浓度的稀硝酸反应,测量合金的质量与产生气体的体积(标准状况),列表如下:
A.A
B.B
C.C
来源:91考试 网D.D
选择题 取不同质量的镁铝合金分别与25mL同浓度的稀硝酸反应,测量合金的质量与产生气体的体积(标准状况),列表如下:
A.A
B.B
C.C
D.D
本题答案:AD
本题解析:分析:分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为224mL×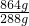 =672mL>560mL,故第3组金属有剩余,硝酸完全反应.
=672mL>560mL,故第3组金属有剩余,硝酸完全反应.
第3个实验后向反应容器内加入足量的1.0mol/L?NaOH(aq)充分反应,使固体质量不再发生变化,使氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2.
根据n=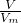 计算第3组生成的NO的物质的量,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的
计算第3组生成的NO的物质的量,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的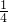 ,据此计算25mL硝酸溶液中n(HNO3)、起酸性作用的硝酸的物质的量,根据c=
,据此计算25mL硝酸溶液中n(HNO3)、起酸性作用的硝酸的物质的量,根据c=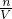 计算原硝酸溶液的浓度;
计算原硝酸溶液的浓度;
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,根据二者质量与转移电子数目列方程计算x、y的值,进而计算864mg合金中Al的物质的量,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2),再根据V=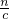 计算需要氢氧化钠溶液的最小体积.
计算需要氢氧化钠溶液的最小体积.
解答:分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为224mL×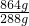 =672mL>560mL,故第3组金属有剩余,硝酸完全反应.
=672mL>560mL,故第3组金属有剩余,硝酸完全反应.
第3个实验后向反应容器内加入足量的1.0mol/L?NaOH(aq)充分反应,使固体质量不再发生变化,使 91EXAm.org氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2.
第3组生成的NO的物质的量为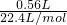 =0.025mol,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的
=0.025mol,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的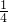 ,故25mL硝酸溶液中n(HNO3)=0.025mol÷
,故25mL硝酸溶液中n(HNO3)=0.025mol÷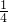
=0.1mol,原硝酸溶液的浓度为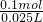 =4mol/L.
=4mol/L.
起酸性作用的硝酸的物质的量为0.1mol-0.025mol=0.075mol,
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,由二者质量与转移电子数目守恒有: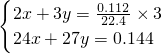
解得x=0.0015,y=0.004,
故864mg合金中Al的物质的量0.004mol×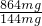 =0.024mol,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为
=0.024mol,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为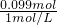 =0.099L=99mL,
=0.099L=99mL,
故选AD.
点评:本题考查混合物的有关计算,过程复杂、计算量较大,题目难度较大,注意利用守恒思想进行的解答.
本题所属考点:【金属及其化合物】
本题难易程度:【困难】