时间:2016-12-18 14:45:32
选择题 将铝粉与某铁的氧化物FeO?2Fe2O3粉末配制成铝热剂,分成两等份.一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为7.84L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
A.5.6L
B.7.84L
C. 11.2L
D.15.68L
选择题 将铝粉与某铁的氧化物FeO?2Fe2O3粉末配制成铝热剂,分成两等份.一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为7.84L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
A.5.6L
B.7.84L
C.11.2L
D.15.68L
本题答案:A
本题解析:分析:分成两等份.一份直接放入足量的烧碱溶液中,只有铝与氢氧化钠发生反应生成氢气,7.84L为氢气体积,根据氢气的体积计算出铝的物质的量.另一份在高温下恰好反应完全,实质为铝置换出铁,铁的氧化物FeO?2Fe2O3中的氧原子全部与铝结合生成氧化铝,利用氧原子守恒,根据铝的物质的量,计算出氧原子的物质的量,再结合氧化物FeO?2Fe2O3的化学式计算出其物质的量,再根据铁原子守恒,可知生成的铁的物质的量.根据铁的物质的量计算铁与盐酸反应生成的氢气体积.
解答:一份直接放入足量的烧碱溶液中,铝与氢氧化钠发生反应生成氢气7.84L,
氢气的物质的量为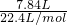 =0.35mol.
=0.35mol.
铁的氧化物FeO?2Fe2O3中的氧原子全部与铝结合生成氧化铝,
所以根据关系式3H2~~~~2Al~~~~3O~~~~Al2O3
?????????????3??????????2???????? 3
????????? ??0.35mol??? 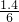 mol????0.35mol
mol????0.35mol
由于氧化物为FeO?2Fe2O3,根据氧原子守恒,所以氧化物FeO?2Fe2O3的为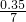 =0.05mol.
=0.05mol.
根据铁原子守恒,可知另一份生成的铁的物质的量为0.05mol×5=0 .25mol.
根据Fe~H2可知,0.25molFe可生成氢气0.25mol,所以另一份生成的氢气的体积为0.25mol×22.4L/mol=5.6L.
故选A.
点评:本题考查混合物的计算、铝的性质,题目难度较大,关键清楚反应过程.本解法在反应的基础上利用原子守恒,简化计算步骤,注意守恒思想的灵活运用.
本题所属考点:【金属及其化合物】
本题难易程度:【困难】