时间:2016-12-18 13:08:47
选择题 100毫升0.3摩尔/升Na2SO4溶液和50毫升0.2摩尔/升Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度为
A.0.20摩尔/升
B.0.25摩尔/升
C.0.40摩尔/升
D.0.50摩尔/升
选择题 100毫升0.3摩尔/升Na2SO4溶液和50毫升0.2摩尔/升Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度为
A.0.20摩尔/升
B.0.25摩尔/升
C.0.40摩尔/升
D.0.50摩尔/升
本题答案:C
本题解析:分析:100毫升0.3摩尔/升Na2SO4溶液和50毫升0.2摩尔/升Al2(SO4)3溶液混合后,Na2SO4 与 Al 91ExAm.org2(SO4)3 混合后不发生反应,故混合溶液中各物质的量是不变的,根据公式c=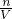 来计算微粒的物质的量浓度.
来计算微粒的物质的量浓度.
解答:100毫升0.3摩尔/升Na2SO4溶液和50毫升0.2摩尔/升Al2(SO4)3溶液混合后,Na2SO4 与 Al2(SO4)3 混合后不发生反应,故混合溶液中各物质的量是不变的,Na2SO4的物质的量为 0.1mL×0.3mol/L=0.03 mol,则(SO4)2-的物质的量为0.03 mol,Al2(SO4)3 的物质的量为:0.05mL×0.2mol/L=0.01 mol,,则(SO4)2-的物质的量为 3×0.01mol=0.03 mol,所以混合后溶液中(SO4)2-的物质的量为0.03mol+0.03mol=0.06mol,混合后溶液的体积可以粗略认为是两溶液混合后体积之和,根据公式c=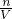 =
=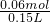 =0.40mol/L,故硫酸根的物质的量浓度为0.40 mol/L,
=0.40mol/L,故硫酸根的物质的量浓度为0.40 mol/L,
故选C.
点评:本题考查物质的量浓度的计算,可以根据公式来计算,是一道基础知识题目.
本题所属考点:【物质的鉴别】
本题难易程度:【一般】