时间:2016-12-18 12:45:20
选择题 向20mL?Na2SO4溶液中加过量的氯化钡溶液,得到2.33g沉淀,原溶液中Na+的物质的量浓度为
A.1.0mol/L
B.2.0mol/L
C.0.50mol/L
D.0.025mol/L
选择题 向20mL?Na2SO4溶液中加过量的氯化钡溶液,得到2.33g沉淀,原溶液中Na+的物质的量浓度为
A.1.0mol/L
B.2.0mol/L
C.0.50mol/L
D.0.025mol/L
本题答案:A
本题解析:分析:Na2SO4溶液中加过量的氯化钡溶液发生SO42-+Ba2+═BaSO4↓,2.33g沉淀为硫酸钡,利用离子方程式可计算硫酸根离子的物质的量,在利用化学式可判断Na+的物质的量,然后计算其浓度.
解答:氯化钡溶液过量,则2.33g沉淀为硫酸钡的质量,其物质的量为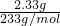 =0.01mol,
=0.01mol,
设Na2SO4的物质的量为x,则
SO42-+Ba2+═BaSO4↓,
?1?????????? 1
?x?????????? 0.01mol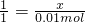 ,解得x=0.01mol,
,解得x=0.01mol,
则Na+的物质的量为0. 91exam.org1mol×2=0.02mol,
原溶液中Na+的物质的量浓度为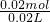 =1.0mol/L,
=1.0mol/L,
故选A.
点评:本题考查学生利用离子反应方程式的计算,明确沉淀质量为硫酸钡质量,利用离子反应可计算硫酸根离子的物质的量是解答本题的关键.
本题所属考点:【化学反应与能量】
本题难易程度:【困难】