时间:2025-06-26 03:49:54
1、选择题 试判断下列哪个装置中灯泡会亮
参考答案:C
本题解析:A项:没有形成闭合回路,灯泡不会亮,故错;B、D项:没有氧化还原反应发生,即没有电荷移动,灯泡不会亮,故错。故选C。
考点:原电池
点评:记住原电池的形成条件是解题的关键,两个电极、电解质溶液、发生氧化还原反应形成闭合回路。
本题难度:简单
2、选择题 下列说法正确的是
[? ]
A.常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则常温下Ksp?(BaCO3)<Ksp(BaSO4)?
B.常温下,向纯水中加入钠或氢氧化钠都能使水的电离平衡逆向移动,水的离子积不变
C.常温下,反应4Fe(OH)2(s)+?O2(g)?+2H2O(l)?=4Fe(OH)3(s)的△H<0、△S<0
D.铅蓄电池在工作过程中,负极质量减少,阳极质量增加
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是
[? ]
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是正极
参考答案:C
本题解析:
本题难度:简单
4、填空题 (10分)如图所示3套实验装置,分别回答下列问题。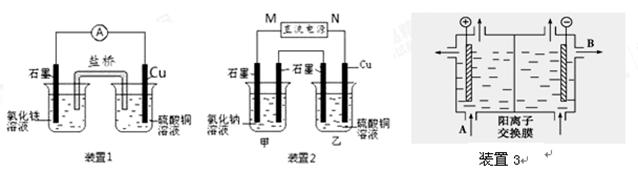
(1)装置1中的Cu是?极(填“正”或“负”),该装置发生的总反应的离子方程式为?。
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为?极
② 乙烧杯中电解反应的离子方程式?。
(3)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理装置3所示。
①请写出A、B两处物质的名称:A___________________B____________________
②请写出电解食盐水的离子方程式__________________________________________
参考答案:(1)负? 2Fe3+ + Cu = 2Fe2+? + Cu2+
(2)?①正?
②2Cu2+ + 2H2O 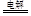 2Cu + O2 ↑ + 4H+
2Cu + O2 ↑ + 4H+
(3) ① A: 饱和NaCl溶液;? B :稀NaOH溶液
② 2Cl- + 2H2O 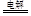 Cl2 ↑+ H2 ↑+ 2OH-
Cl2 ↑+ H2 ↑+ 2OH-
本题解析:⑴装置1为原电池,铜为负极,被氧化,石墨正极,其电池总反应为2Fe3++Cu═2Fe2++Cu2+;
⑵向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,说明甲中右边电极反应生成OH-,该极应为电解池的阴极,则M为电源的正极,N为电源的负极,由此可知甲为电解食盐水装置,而乙为电解硫酸铜溶液的装置,其阳极生成氧气,阴极生成铜,则电解的离子方程式为2Cu2++2H2O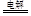 2Cu+O2↑+4H+;
2Cu+O2↑+4H+;
⑶根据电解池中阴离子移向阳极,阳离子移向阴极,图示装置中的交换膜是阳离子交换膜,A出口主要是饱和NaCl溶液,B出口主要是氢氧化钠溶液,甲装置是电解饱和食盐水,电解氯化钠溶液时生成氢氧化钠和氢气、氯气,其电解反应的离子方程式为:2Cl-+2H2O Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
本题难度:一般
5、填空题 有甲、乙、丙、丁四种金属,把甲、丙浸入稀硫酸中,用导线连接时丙为负极;把乙、丁分别浸入稀硫酸中,丁产生气泡的速率更大;把甲、乙用导线连接浸入稀硫酸中,甲上有气泡冒出;把丙浸入丁的硝酸盐溶液中,丙的表面有丁析出。这四种金属的活动性由强到弱的顺序是
参考答案:丙丁乙甲
本题解析:原电池中较活泼的金属作负极,所以丙的金属性强于甲的。丁产生气泡的速率更大,说明丁的金属性强于乙的。把甲、乙用导线连接浸入稀硫酸中,甲上有气泡冒出,说明甲是正极,因此金属性是乙大于甲。把丙浸入丁的硝酸盐溶液中,丙的表面有丁析出,说明丙的金属性强于丁的,所以这四种金属的活动性由强到弱的顺序是.丙丁乙甲。
本题难度:一般