时间:2025-06-26 03:42:44
1、选择题 25℃时,将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1∶100混合,反应后所得溶液pH=7。若x= y,则x值为
y,则x值为
A.2
B.3
C.4
D.5
2、选择题 下列溶液中,微粒浓度关系正确的是(?)
A.含NH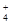 、Cl-、H+、OH-的溶液,其离子浓度一定是:c(Cl-)>c(NH+4)>c(H+)>c(OH-)
、Cl-、H+、OH-的溶液,其离子浓度一定是:c(Cl-)>c(NH+4)>c(H+)>c(OH-)
B.pH=7的氨水与氯化铵的混合溶液中,Cl-与NH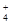 的浓度关系:c(Cl-)>c(NH
的浓度关系:c(Cl-)>c(NH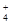 )
)
C.0.1 mol・L-1的Na2S溶液中粒子浓度关系:c(OH-)=c(HS-)+2c(H2S)+c(H+)
D.pH=3的一元酸和pH=11的一元强碱等体积混合:c(OH-)=c(H+)
3、选择题 常温下,将a mol/L的MOH(可溶性弱碱)与b mol/L盐酸等体积混合,已知相同条件下MOH的电离程度大于M+的水解程度,则下列有关推论不正确的是( )
A.若混合后溶液pH=7,则c(M+)=c(Cl-)
B.若b=2a,则c(Cl-)>c(M+)>c(H+)>c(OH-)
C.若a=2b,则c(M+)>c(Cl-)>c(OH-)>c(H+)
D.若混合后溶液满足c(H+)=c(OH-)+c(MOH),则可推出a=b
4、选择题 常温下,有四种溶液:
| ① | ② | ③ | ④ |
| 0.1mol/L CH3COOH溶液 | pH = 12 NaOH溶液 | 0.1mol/L NaOH溶液 | pH = 2 CH3COOH溶液 |
5、选择题 下列选项中说明乙醇作为燃料的优点的是( )
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境 ③乙醇是一种再生能源 ④燃烧时放出大量热量
A.①②③
B.①②④
C.①③④
D.②③④