时间:2025-06-26 03:41:54
1、选择题 下列气体能用启普发生器制取的是
[? ]
A.O2?
B.C2H4
C.C2H2?
D.H2
参考答案:D
本题解析:
本题难度:简单
2、简答题 (Ⅰ)甲、乙、丙三位同学分别用如下实验装置及化学药品(碱石灰为氢氧化钠和生石灰的混合物)制取氨气.请你参与探究,并回答问题: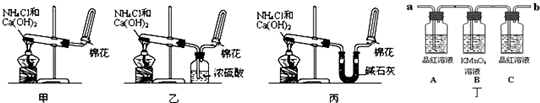
(1)甲、乙、丙三位同学制取氨气的化学方程式为:______.
(2)他们都用向下排空气法收集氨气,其原因是______.
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是______(填“甲”、“乙”或“丙”).
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论):______.
(5)三位同学都认为自己的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的是______(填“甲”、“乙”或“丙”),该装置中的NH4HCO3固体能否用NH4Cl固体代替?______(填“能”或“不能”).
(Ⅱ)已知二氧化硫可使高锰酸钾溶液褪色.反应的化学方程式为:
5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4
如图丁为验证浓硫酸与木炭在加热条件下,反应产物中是否含有SO2和CO2的部分装置.
(1)实验时,从______端连接盛有澄清石灰水的实验装置(用a或b填空).
(2)可观察到A瓶的溶液______.
(3)C瓶溶液的作用是______.
参考答案:(I)(1)在加热条件下,氯化铵和氢氧化钙反应生成氯化钙、氨气和水,反应方程式为:2NH4Cl+Ca(OH)2△.CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2△.CaCl2+2NH3↑+2H2O;
(2)氨气密度小于空气且和空气不反应,所以可以采用向下排空气法收集,故答案为:NH3的密度小于空气;
(3)氨气属于碱性气体,能和酸反应,氨气通过浓硫酸时会被氧化,所以乙不能收集到氨气,故答案为:乙;
(4)氨气能使湿润的红色石蕊试纸变蓝色,也能和氯化氢反应生成氯化铵而产生白烟,其检验方法为:将湿润的红色石蕊试纸置于管口,若试纸变蓝,则说明已收集满(或用蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,则证明已收集满),
故答案为:将湿润的红色石蕊试纸置于管口,若试纸变蓝,则说明已收集满(或用蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,则证明已收集满);
(5)碳酸氢铵分解生成二氧化碳、氨气和水,要收集纯净的氨气,应除去二氧化碳和水蒸气,可以将生成的气体通过碱石灰除去二氧化碳和水蒸气,所以丙能实现;氯化铵在加热条件下分解生成氨气和氯化氢,在试管口氯化氢和氨气反应生成氯化铵固体,所以得不到氨气,故答案为:丙;不能;
(II)(1)洗气装置中导气管遵循“长进短出”的原则,所以a端气体进入进行检验,b端连接盛有澄清石灰水的实验装置用于检验是否存在CO2气体,故答案为:b;
(2)二氧化硫能使品红溶液褪色,所以将混合气体通过品红溶液时,品红溶液褪色,故答案为:褪色;
(3)C装置是检验二氧化硫是否除尽,如果还有二氧化硫则C中品红溶液褪色,故答案为:检验SO2是否除尽.
本题解析:
本题难度:简单
3、选择题 下列制备和收集气体的实验装置合理的是?
[? ]
A.用氯化铵制NH3 ?
?
B.用铜片和稀硝酸制NO?  ?
?
C.用锌粒和稀硫酸制H2? ?
?
D.用双氧水和二氧化锰制O2
参考答案:D
本题解析:
本题难度:简单
4、实验题 甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与研究,并回答有关问题
(1)三位同学所用化学药品制取氨气的化学方程式为_________________________。
(2)三位同学都用向下排空气法而不用其他实验室常用方法收集氨气,其原因是________________。
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气,如果他的实验操作都正确,你认为没有收集到氨气的同学是_________(填“甲”、“乙”或“丙”),收集不到氨气的主要原因是
___________________________。
(4)你检验氨气是否收集满的方法是(简述操作方法、现象和结论)___________________________。
(5)三位同学都认为他们的实验装置也可用加热碳酸氢铵固体制取氨气,你判断他们能够达到实验目的的是_____(填“甲”、“乙”或“丙”),其理由是___________________________。
参考答案:(1)2NH4Cl+Ca(OH)2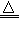 CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
(2)氨气密度比空气小,易溶于水
(3)乙;氨气被浓硫酸吸收
(4)将一张湿润的红色石蕊试纸放在收集氨气的试管下口,若试纸变蓝说明氨气已收集满
(5)丙;碱石灰能除去二氧化碳和水蒸气
本题解析:
本题难度:一般
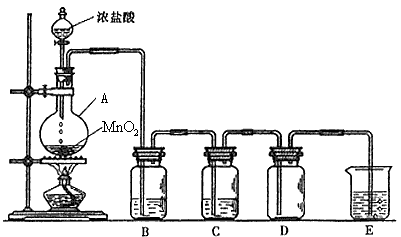
5、实验题 实验室用浓盐酸和二氧化锰反应制取纯净、干燥的氯气(氯化氢极易溶于水),装置如下图所示:
参考答案:(1)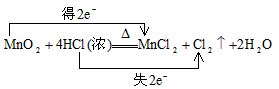 ;1:2
;1:2
(2)水(饱和食盐水) ;浓硫酸 ;氢氧化钠溶液;除去Cl2中混有的气体 ;除去氯气中的水(干燥氯气) ;吸收多余的氯气,防止污染空气
(3)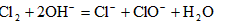
本题解析:
本题难度:一般